万双林医生的科普号
- 精选 强直性脊柱炎的诊治进展
强直性脊柱炎的诊治进展强直性脊柱炎(AS)是以骶髂关节和脊柱附着点炎症为主要症状的疾病。与HLA-B27呈强关联。某些微生物(如克雷白杆菌)与易感者自身组织具有共同抗原,可引发异常免疫应答。是四肢大关节,以及椎间盘纤维环及其附近结缔组织纤维化和骨化,以及关节强直为病变特点的慢性炎性疾病。强直性脊柱炎属风湿病范畴,病因尚不明确,是以脊柱为主要病变部位的慢性病,累及骶髂关节,引起脊柱强直和纤维化,造成不同程度眼、肺、肌肉、骨骼病变,是自身免疫性疾病。一、病因很可能在遗传因素的基础上的受环境因素(包括感染)等多方面的影响而致病。遗传因素在AS的发病中具有重要作用。一般认为和HLA-B27有直接关系,HLA-B27阳性者AS发病率为10%~20%,免疫因素也是其中一个病因,有人发现60%AS患者血清补体增高,大部分病例有IgA型类湿因子,血清C4和IgA水平显著增高。创伤、内分泌、代谢障碍和变态反应等亦被疑为发病因素。二、临床表现1.初期症状对于16~25岁青年,尤其是青年男性。强直性脊柱炎一般起病比较隐匿,早期可无任何临床症状,有些病人在早期可表现出轻度的全身症状,如乏力、消瘦、长期或间断低热、厌食、轻度贫血等。由于病情较轻,病人大多不能早期发现,致使病情延误,失去最佳治疗时机。2.关节病变表现AS病人多有关节病变,且绝大多数首先侵犯骶髂关节,以后上行发展至颈椎。少数病人先由颈椎或几个脊柱段同时受侵犯,也可侵犯周围关节,早期病变处关节有炎性疼痛,伴有关节周围肌肉痉挛,有僵硬感,晨起明显。也可表现为夜间疼,经活动或服止痛剂缓解。随着病情发展,关节疼痛减轻,而各脊柱段及关节活动受限和畸形,晚期整个脊柱和下肢变成僵硬的弓形,向前屈曲。(1)骶髂关节炎约90%AS病人最先表现为骶髂关节炎。以后上行发展至颈椎,表现为反复发作的腰痛,腰骶部僵硬感,间歇性或两侧交替出现腰痛和两侧臀部疼痛,可放射至大腿,无阳性体征,伸直抬腿试验阴性。但直接按压或伸展骶髂关节可引起疼痛。有些病人无骶髂关节炎症状,仅X线检查发现有异常改变。约3%AS颈椎最早受累,以后下行发展至腰骶部,7%AS几乎脊柱全段同时受累。(2)腰椎病变腰椎受累时,多数表现为下背部和腰部活动受限。腰部前屈、背伸、侧弯和转动均可受限。体检可发现腰椎脊突压痛,腰椎旁肌肉痉挛;后期可有腰肌萎缩。(3)胸椎病变胸椎受累时,表现为背痛、前胸和侧胸痛,最常见为驼背畸形。如肋椎关节、胸骨柄体关节、胸锁关节及肋软骨间关节受累时,则呈束带状胸痛,胸廓扩张受限,吸气咳嗽或打喷嚏时胸痛加重。严重者胸廓保持在呼气状态,胸廓扩张度较正常人降低50%以上,因此只能靠腹式呼吸辅助。由于胸腹腔容量缩小,造成心肺功能和消化功能障碍。(4)颈椎病变少数病人首先表现为颈椎炎,先有颈椎部疼痛,沿颈部向头部臂部放射。颈部肌肉开始时痉挛,以后萎缩,病变进展可发展至颈胸椎后凸畸形。头部活动明显受限,常固定于前屈位,不能上仰、侧弯或转动。严重者仅能看到自己足尖前方的小块地面,不能抬头平视。(5)周围关节病变约半数AS病人有短暂的急性周围关节炎,约25%有永久性周围关节损害。一般多发生于大关节,下肢多于上肢。肩关节受累时,关节活动受限,疼痛更为明显,梳头、抬手等活动均受限。侵犯膝关节时则关节呈代偿性弯曲,使行走、坐立等日常生活更为困难。极少侵犯肘、腕和足部关节。此外,耻骨联合亦可受累,骨盆上缘、坐骨结节、股骨大粗隆及足跟部可有骨炎症状,早期表现为局部软组织肿、痛,晚期有骨性粗大。一般周围关节炎可发生在脊柱炎之前或以后,局部症状与类风湿关节炎不易区别,但遗留畸形者较少。3.关节外表现AS的关节外病变,大多出现于脊柱炎后,偶有骨骼肌肉症状之前数月或数年发生关节外症状。AS可侵犯全身多个系统,并伴发多种疾病。(1)心脏病变以主动脉瓣病变较为常见。临床有不同程度主动脉瓣关闭不全者约1%;约8%发生心脏传导阻滞,可与主动脉瓣关闭不全同时存在或单独发生,严重者因完全性房室传导阻滞而发生阿—斯综合征。当病变累及冠状动脉口时,可发生心绞痛。少数发生主动脉肌瘤、心包炎和心肌炎。(2)眼部病变长期随访,25%AS病人有结膜炎、虹膜炎、眼色素层炎或葡萄膜炎,后者偶可并发自发性眼前房出血。虹膜炎易复发,病情越长发生率愈高,但与脊柱炎的严重程度无关,有周围关节病者常见,少数可先于脊柱炎发生。眼部疾病常为自限性,有时需用皮质激素治疗,有的未经恰当治疗可致青光眼或失明。(3)耳部病变在发生慢性中耳炎的AS病人中,其关节外表现明显多于无慢性中耳炎的AS病人。(4)肺部病变少数AS病人后期可并发上肺叶斑点状不规则的纤维化病变,表现为咳痰、气喘,甚至咯血,并可能伴有反复发作的肺炎或胸膜炎。(5)神经系统病变由于脊柱强直及骨质疏松,易使颈椎脱位和发生脊柱骨折,从而引起脊髓压迫症。如发生椎间盘炎则引起剧烈疼痛。AS后期可侵犯马尾,发生马尾综合征,而导致下肢或臀部神经根性疼痛,骶神经分布区感觉丧失,跟腱反射减弱及膀胱和直肠等运动功能障碍。(6)淀粉样变为AS少见的并发症。(7)肾及前列腺病变与RA相比,AS极少发生肾功能损害,但有发生IgA肾病的报告。AS并发慢性前列腺炎较对照组增高,其意义不明。三、检查1.电子计算机断层扫描(CT)对于临床怀疑而X线不能确诊者,可以行CT检查,它能清晰显示骶髂关节间隙,对于测定关节间隙有无增宽、狭窄、强直或部分强直有独到之处。2.磁共振(MRI)和单光子发射计算机断层扫描(SPECT)研究者认为,MRI和SPECT闪烁造影骶髂关节拍片,非常有助于极早期诊断和治疗,从这个角度看明显优于普通X线,但费用昂贵,不提倡作为常规检查。3.实验室检查白细胞计数正常或升高,淋巴细胞比例稍增加,少数病人有轻度贫血(正细胞低色素性),血沉可增快,但与疾病活动的相关性不大,而C反应蛋白则较有意义。血清白蛋白减少,α1和γ球蛋白增加,血清免疫球蛋白IgG、IgA和IgM可增加,血清补体C3和C4常增加。约50%病人碱性磷酸酶升高,血清肌酸磷酸激酶也常升高。血清类风湿因子阴性。虽然90%~95%以上AS病人HLA-B27阳性,但一般不依靠HLA-B27来诊断AS,HLA-B27不作常规检查。4.X线检查对AS的诊断有极为重要的意义,98%~100%病例早期即有骶髂关节的X线改变,是本病诊断的重要依据。早期X线表现为骶髂关节炎,病变一般在骶髂关节的中下部开始,为两侧性。开始多侵犯髂骨侧,进而侵犯骶骨侧。可见斑点状或块状,髂骨侧明显。继而可侵犯整个关节,边缘呈锯齿状,软骨下有骨硬化,骨质增生,关节间隙变窄。最后关节间隙消失,发生骨性强直。骶髂关节炎X线诊断标准分为5期:0级为正常骶髂关节,Ⅰ期为可疑骶髂关节炎,Ⅱ期为骶髂关节边缘模糊,略有硬化和微小侵袭病变,关节间隙无改变,Ⅲ期为中度或进展性骶髂关节炎,伴有一项(或以上)变化:近关节区硬化、关节间隙变窄/增宽、骨质破坏或部分强直,Ⅳ期为关节完全融合或强直伴或不伴硬化。脊柱病变的X线表现,早期为普遍性骨质疏松,椎小关节及椎体骨小梁模糊(脱钙),椎体呈“方形椎”,腰椎的正常前弧度消失而变直,可引起一个或多个椎体压缩性骨折。病变发展至胸椎和颈椎椎间小关节,间盘间隙发生钙化,纤维环和前纵韧带钙化、骨化、韧带骨赘形成,使相邻椎体连合,形成椎体间骨桥,呈最有特征的“竹节样脊柱”。原发性AS和继发于炎性肠病、Reiter综合征、银屑病关节炎等伴发的脊柱炎,X线表现类似,但后者为非对称性强直。在韧带、肌腱、滑囊附着处可出现骨质糜烂和骨膜炎,最多见于跟骨、坐骨结节、髂骨嵴等。其他周围关节亦可发生类似的X线变化。四、诊断1.临床表现(1)腰和(或)脊柱、腹股沟、臀部或下肢酸痛不适,或不对称性外周寡关节炎、尤其是下肢寡关节炎,症状持续≥6周。(2)夜间痛或晨僵明显。(3)活动后缓解。(4)足跟痛或其他肌腱附着点病。(5)虹膜睫状体炎的临床表现或既往史。(6)AS家族史或HLA-B27阳性。(7)非甾体抗炎药(NSAIDs)能迅速缓解症状。2.体格检查4字试验,判断患者骶髂关节受累。明显阳性,提示患者骶髂关节间隙有变窄或者有关节的融合。4字试验时患者有明显的疼痛,提示患者骶髂关节有炎症病变。骨盆挤压试验,判断髂关节炎症病变的情况,有局部炎症明显的患者,正压试验是阳性的,而且疼痛明显。指地距,判断患者的腰椎活动度。胸廓活动度,判断胸椎的椎体是否有累及,以及活动情况。枕墙距,判断颈椎出现了受累的表现。3.影像学或病理学(1)双侧X线骶髂关节炎≥Ⅲ期。(2)双侧CT骶髂关节炎≥Ⅱ期。(3)CT骶髂关节炎不足Ⅱ级者,可行MRI检查。如表现软骨破坏、关节旁水肿和(或)广泛脂肪沉积,尤其动态增强检查关节或关节旁增强强度>20%,且增强斜率>10%/min者。(4)骶髂关节病理学检查显示炎症者。4.实验室检查HLA-B27,CRP、ESR,>90%的AS患者HLA-B27阳性5.诊断符合临床标准第1项及其他各项中之3项,以及影像学、病理学标准之任何一项者,可诊断AS。AS病变特点是从骶髂关节开始,沿脊椎缓慢向上进展,或同时向下蔓延。主要表现为腰背痛和晨僵,中晚期伴有脊柱强直、畸形及严重活动受限。部分患者出现外周关节炎,可累及眼、皮肤、肠道、心脏、肺等器官。AS早期病理性标志为骶髂关节炎,脊柱受累晚期的典型表现为“竹节样改变”。国外研究,仅13.7%因背痛就诊的AS患者首诊被确诊,我国研究显示AS的误诊率高达82%,我国AS患者平均延迟诊断时间长达6年,首诊最常见的诊断为椎间盘突出症。五、鉴别诊断(一)常见疾病鉴别1.腰骶关节劳损慢性腰骶关节劳损为持续性、弥漫性腰痛,以腰骶部最重,脊椎活动不受限,X线无特殊改变。急性腰骶关节劳损,疼痛因活动而加重,休息后可缓解。2.骨关节炎常发生于老年人,特征为骨骼及软骨变性、肥厚,滑膜增厚,受损关节以负重的脊柱和膝关节等较常见。累及脊椎者常以慢性腰背痛为主要症状,与AS易混淆。但本病不发生关节强直及肌肉萎缩,无全身症状,X线表现为骨赘生成和椎间隙变窄。3.Forestier病(老年性关节强直性骨肥厚)脊椎亦发生连续性骨赘,类似AS的脊椎竹节样变,但骶髂关节正常,椎间小关节不受侵犯。4.结核性脊椎炎临床症状如脊椎疼痛、压痛、僵硬、肌肉萎缩、驼背畸形、发热、血沉快等与AS相似,但X线检查可资鉴别。结核性脊柱炎时,脊椎边缘模糊不清,椎间隙变窄,前楔形变,无韧带钙化,有时有脊椎旁结核脓疡阴影存在,骶髂关节为单侧受累。5.类风湿关节炎现已确认AS不是RA的一种特殊类型,两者有许多不同点可资鉴别。RA女性多见,通常先侵犯手足小关节,且呈双侧对称性,骶髂关节一般不受累,如侵犯脊柱,多只侵犯颈椎,且无椎旁韧带钙化,有类风湿皮下结节,血清RF常阳性,HLA-B27抗原常阴性。6.肠病性关节病溃疡性结肠炎、Crohn病或肠原性脂肪代谢障碍(Whipple)都可发生脊柱炎,且肠病性关节病受累关节和X线改变与AS相似而不易区别,因此需要寻找肠道症状和体征,以资鉴别。溃疡性结肠炎有结肠黏膜溃疡、水肿及血性腹泻。Crohn病有腹痛、营养障碍及瘘管形成。Whipple病有脂肪泻,急剧消瘦等。这些都有助于原发性疾病的诊断。肠病性关节病HLA-B27阳性率低,Crohn病病人肠灌注液IgG增高,而AS病人肠灌液中IgG基本正常。7.Reiter综合征和银屑病关节炎两病均可发生脊柱炎和骶髂关节炎,但脊柱炎一般发生较晚,较轻,椎旁组织钙化少,韧带骨赘以非边缘型为主(纤维环外纤维组织钙化),在相邻两椎体间形成部分性骨桥与AS的竹节样脊柱不同。骶髂关节炎一般为单侧性或双侧非对称损害,银关节炎则有皮肤银屑病损害等可资鉴别。8.肿瘤肿瘤亦可引起进行性疼痛,需作全面检查,明确诊断,以免误诊。9.急性风湿热部分病人初期临床表现颇似急性风湿热,或出现大关节肿痛,或伴有长期低热、体重减轻,以高热和外周关节急性炎症为首发症状的也不少见,此类病人多见于青少年,也容易被长期误诊。10.结核病个别病人初期类似结核病,表现为低热、盗汗、虚弱、乏力、体重减轻、贫血,有时伴有单侧髋关节炎症,易被误诊为结核病。有关的结核检查可鉴别。(二)与血清阴性脊柱关节病鉴别1.Reiter综合征和银屑病关节炎可发生脊柱炎和骶髂关节炎,但脊柱炎一般发生较晚,较轻,椎旁组织钙化少,韧带骨赘以非边缘型为主(纤维环外纤维组织钙化),在相邻两椎体间形成部分性骨桥与强直性脊柱炎的竹节样脊柱不同。骶髂关节炎一般为单侧性或双侧非对称性,棘突关节病变少见,无普遍性骨质疏松。另外,Reiter综合征有结膜炎、尿道炎、黏膜皮肤损害,银屑病关节炎则有皮肤银屑病损害等可供鉴别。2.肠病性关节炎溃疡性结肠炎、Crohn病、肠原性脂肪代谢障碍(Whippe)都可发生脊柱炎,且肠病性关节病受累关节和X线改变与强直性脊柱炎相似而不易区别,因此需要寻找肠道症状和体征,以资鉴别。溃疡性结肠炎有结肠黏膜溃疡、水肿及血性腹泻,Crohn病有腹痛、营养障碍及痿管形成,Whipple病有脂肪泻,急剧消瘦等。肠病性关节病HLA-B27阳性率低,Crohn病病人肠灌注液IgG增高,而强直性脊柱炎病人肠灌液中IgG基本正常。3.反应性关节炎常继发于身体其他部位感染后出现,一般可以发现感染灶,抗生素有效。六、治疗1.控制AS治疗的目的在于控制炎症,减轻或缓解症状,维持正常姿势和最佳功能位置,防止畸形。要达到上述目的,关键在于早期诊断早期治疗,采取综合措施进行治疗,包括教育病人和家属、体疗、理疗、药物和外科治疗等。未及时治疗或治疗不当,三年致残率约为45.5%,五年致残率高达70%以上。控制疾病进展,降低残疾的关键在于早期诊断以及合理及时的治疗。早期-药物治疗,晚期关节变形-手术治疗(1)该病治疗从教育病人和家属着手,使其了解疾病的性质、大致病程、可能采用的措施以及将来的预后,以增强抗病的信心和耐心,取得他们的理解和密切配合。(2)注意日常生活中要维持正常姿势和活动能力,如行走、坐位和站立时应挺胸收腹,睡觉时不用枕或用薄枕,睡硬木板床,取仰卧位或俯卧位,每天早晚各俯卧半小时。参与力所能及的劳动和体育活动。工作时注意姿势,防止脊柱弯曲畸形等。(3)保持乐观情绪,消除紧张、焦虑、抑郁和恐惧的心理;戒烟酒;按时作息,参加医疗体育锻炼。(4)了解药物作用和副作用,学会自行调整药物剂量及处理药物副作用,以利配合治疗,取得更好的效果。2.体疗体育疗法对各种慢性疾病均有好处,对AS更为重要。可保持脊柱的生理弯曲,防止畸形。保持胸廓活动度,维持正常的呼吸功能。保持骨密度和强度,防止骨质疏松和肢体废用性肌肉萎缩等。病人可根据个人情况采取适当的运动方式和运动量。如新的疼痛持续2小时以上不能恢复,则表明运动过度,应适当减少运动量或调整运动方式。3.物理治疗理疗一般可用热疗,如热水浴、水盆浴或淋浴、矿泉温泉浴等,以增加局部血液循环,使肌肉放松,减轻疼痛,有利于关节活动,保持正常功能,防止畸形。4.药物治疗(1)非甾体类抗炎药有消炎止痛、减轻僵硬和肌肉痉挛作用。副作用为胃肠反应、肾脏损害、延长出血时间等。妊娠及哺乳期妇女,更应特别注意。(2)柳氮磺胺吡啶SSZ是5-氨基水杨酸(5-ASA)和磺胺吡啶(SP)的偶氮复合物,80年代开始用于治疗AS。副作用主要为消化道症状、皮疹、血象及肝功改变等,但均少见。用药期间宜定期检查血象及肝肾功能。(3)甲氨蝶呤据报道疗效与SSZ相似。口服和静脉用药疗效相似。副作用有胃肠反应、骨髓抑制、口腔炎、脱发等,用药期间定期查肝功和血象,忌饮酒。(4)肾上腺皮质激素一般情况下不用肾上腺皮质激素治疗AS,但在急性虹膜炎或外周关节炎用NSAIDs治疗无效时,可用CS局部注射或口服。(5)雷公藤多甙有消炎止痛作用,服用方便。副作用有胃肠反应、白细胞减少、月经紊乱及精子活力降低等,停药后可恢复。(6)生物制剂快速控制炎症水平、缓解患者症状、抑制疾病进展、提高患者生活质量。TNFi(肿瘤坏死因子(TNF-α)拮抗剂)等(如益赛普、阿达木单抗等)和IL-17抑制剂(如司库奇尤单抗)是治疗AS等脊柱关节疾病的最佳选择,司库奇尤单抗是最新的生物制剂,疗效确切、副作用小。司库奇尤单抗长期治疗AS,炎性肠病、主要心血管不良事件、感染等不良反应发生率低,无结核再激活的报告。有条件者应尽量尽早选择。5.手术治疗严重脊柱驼背、畸形,待病情稳定后可作矫正手术,腰椎畸形者可行脊椎截骨术矫正驼背。对颈7胸1截骨术可矫正颈椎严重畸形。七、预防1.应避免强力负重,使病变加重。避免长时间维持一个姿势不动。若要长时间坐着时,至少每小时要起来活动十分钟。勿用腰背束缚器(会减少活动),使脊椎炎恶化。2.睡眠时避免垫枕头且不睡软床。睡觉时最好是平躺保持背部直立。3.清晨起床背脊僵硬时,可以热水浴来改善。热敷对于缓解局部疼痛亦有部分疗效。不抽烟,以免造成肺部伤害。4.慎防外伤,开车时一定系上安全带,尽量不要骑机动车。5.在寒冷、潮湿季节中,更应防范症状复发。6.胃肠道及泌尿道的感染常诱发脊椎炎,故应该注意饮食卫生,多喝开水,多吃青菜水果,避免憋尿及便秘。7.注意其他家族成员有无强直性脊柱炎的症状,如下背酸痛,晨间僵硬等。若有,应尽早就医。
 万双林 主任医师 邵逸夫医院 骨科70人已读
万双林 主任医师 邵逸夫医院 骨科70人已读 - 精选 椎体血管瘤的诊治策略
1.概述(background)血管瘤(hemangioma)是血管来源的良性生长的肿瘤,通常好发皮肤,皮下组织及粘膜等人体结构,骨骼内生长亦较多见。1867年,Virchow首先发现并描述了椎体血管瘤(vertebral hemangioma,VH),1917年Hitzor首先描述了血管瘤在平片上的表现,1926年Perman等首先描述了经病理证实的椎体血管瘤在X片上的影像学表现。2.流行病学(epidemiology)据Shchmorl等通过3000余列尸检发现椎体血管瘤在人体中的发病率约11%,但2009 Barzin等通过对伊朗约782例随机抽取的MRI进行分析发现伊朗约26.9%有椎体血管瘤的影像学表现。大部分人群椎体血管瘤终身无症状,仅体检时偶然发现,仅有约1%出现临床症状,30-50岁者为临床症状好发期,发生于青春期及怀孕期妇女也有较多报道,Mohan等报道一例椎体血管瘤最小发病年龄10岁。该病通常女性多于男性,报道比例2:1到4:1不等。椎体血管瘤好发胸椎,其次为腰椎及颈椎,约10%-15%累及脊椎后结构,合并脊髓硬膜外或硬膜下血管瘤者偶有报道。约1/3椎体血管瘤单节椎体,约1/3累及两节及以上椎体,累及5节以上椎体者罕见。目前国内尚无椎体血管瘤大样本多中心的发病率报道。3.病因学(etiology)椎体血管瘤目前发病原因尚不明确,通常认为椎体血管瘤与胚胎血管先天发育不良相关。病理学上主要分为毛细血管血管瘤,海绵状血管瘤两大类,血管瘤由薄层扁平的处于静止期的血管内皮细胞组成血管管腔。鉴于椎体血管瘤好发女性,同时有较多报道怀孕妇女孕期最后3月较易诱发症状,有学者提出雌激素与血管瘤发病相关可能性,但Schwartz等报道一例29岁孕期妇女椎体血管瘤切除后行病理检测雌激素受体,结果阴性,相关性有待实验进一步研究。4.影像学表现(image)椎体血管瘤影像学上较特异性表现:X片上表现为椎体内垂直增粗的骨小梁,形似蜂巢样改变;CT上可见斑点样骨小梁增粗改变,Laredo等总结若椎体血管瘤在CT中有以下:①T3-T9节段、②累及整个椎体、③病变扩展至椎弓、④椎体皮质骨破坏、⑤椎体上不规则蜂巢样骨小梁、⑥软组织肿块等三个或三个以上改变或有神经痛、脊髓压迫症状则强烈提示病变具有侵袭性,此时需警惕椎体压缩性骨折的发生;MR可以作为血管瘤的确诊诊断,其较特异的表现为上椎体出现混杂的高T1及高T2信号改变,MR上特异性表现被认为与脂肪细胞相关,Laredo等认为在MR中以脂肪信号改变为主的高信号椎体血管瘤提示侵袭性弱,可能以疼痛表现为主;而软组织信号改变为主的低信号椎体血管瘤则提示侵袭性强,较易出现脊髓压迫症状,Kato[17]VH全切术后病理检查与上述结论相一致。核医学检查如SPECT[18]等有报道应用于椎体血管瘤诊断,但因无特异性表现,同时价格昂贵,现通常不应用于椎体血管瘤的诊断,但偶有报道应用于常规影像学检查不能鉴别是否为椎体恶性肿瘤的病人中[19-21]。5.临床症状(symptoms)椎体血管瘤仅有约1%患者出现症状,其中疼痛(60%)及神经功能障碍(30%)为较多见症状;因VH椎体改变为骨小梁增粗,能保持椎体结构的稳定,因此椎体压缩性骨折(10%)较少见,但若影像学如CT或MR上表现为活动性病变,则椎体骨折有较高发生概率[22]。椎体血管瘤产生症状的原因通常认为是血管瘤反复出血,栓塞,机化,再通等使受累椎体本身扩张压迫神经,肿瘤组织突出椎体至神经压迫,椎体结构破坏至椎体压缩性骨折压迫神经。6.临床分型(clincal types)为了便于临床治疗,有学者建议据患者症状可将椎体血管瘤分为四型:Ⅰ无症状性椎体血管瘤(asymptomatic vertebral hemangioma,AVH);Ⅱ局灶性症状(local symptom)而无脊髓压迫(spinal compression);Ⅲ有脊髓压迫(spinal compression)而无横断性损伤(transverse lesion)Ⅳ脊髓压迫引发横断性损伤如截瘫等,一般均由椎体压缩性骨折造成。后三种分类可归类为症状性椎体血管瘤(symptomatic vertebral hemangioma,SVH)。如前所述,VH在影像学表现为非侵袭性,侵袭性时,表现为侵袭性时可伴有较高椎体压缩性骨折的发生率,因此笔者建议据患者影像学表现将Ⅱ、Ⅲ型椎体血管瘤再细分为非侵袭性与侵袭性,及椎体压缩性骨折等3个亚型;IV型椎体血管瘤一般均由椎体压缩性骨折或侵袭性软组织肿块引起,其他原因少见,可将IV分为侵袭性与椎体压缩性2个亚型。VH治疗后症状缓解不明显或复发报道较多,因与首发处理原则不同,建议将复发性或难治性椎体血管瘤单独归类为Ⅴ型(表1)。 表1:椎体血管瘤分型分型亚型Ⅰ:无症状性椎体血管瘤症状性椎体血管瘤非侵袭性侵袭性椎体压缩性骨折Ⅱ:局灶性症状而无脊髓压迫ⅡaⅡbⅡcⅢ:脊髓压迫而无横断性损伤ⅢaⅢbⅢcⅣ:脊髓横断性损伤如截瘫ⅣaⅣbⅤ:复发性或难治性症状性椎体血管瘤7.治疗(treatment)VH只有少数发病,因此对于I型即AVH,目前普遍观点认为无需治疗,只需定期随访。症状性VH认为需要治疗,但对于应用何种方法治疗尚有争议。目前治疗椎体血管瘤的方法主要有:经皮椎体病灶内注射无水乙醇法(ethanol injection),经动脉椎体血管瘤栓塞法(transarterial embolization),经皮椎体成型法(vertebroplasty),放疗(radiotherapy),手术治疗(surgery)。1)经皮椎体病灶内注射无水乙醇法(ethanol injection):1989年Yakes[28]等首先应用病灶内注射无水乙醇的方法治疗2例肌肉血管瘤。后1994年Heiss等将上述方法首先应用与症状性椎体血管瘤的治疗中,取得较好效果。目前国内尚无单纯应用乙醇注射法治疗椎体血管瘤的病案报道。注射乙醇法通过灭活血管瘤官腔的细胞达到去血管化的目的,减轻因血管瘤充血或栓塞造成的肿瘤组织扩张而形成的神经压迫。Heiss等共报道52例VH,其中脊髓压迫症状者共计28例,严重疼痛者1列,未分类者24例,无影像学分类资料。经单侧或双侧椎弓根穿刺入椎体注射无水乙醇,只有1例症状无明显改善。术后随访1月-3年不等,行MR或CT检查,其中5例并发压缩性骨折(随访1月-5月不等)后行手术治疗,1例疼痛复发(随访1月),治疗有效率约85%。乙醇注射法术后较为常见的并发症为椎体压缩性骨折。在上述病例报道中发生椎体压缩性骨折的5例病例无水乙醇注射剂量40-50ml之间,而未发生压缩性骨折的无水乙醇注射量10-15ml,手术后病理学检查见椎体骨坏死,提示并发椎体压缩性骨折与乙醇注射剂量相关。Hesis及Doppman等推荐乙醇注射剂量10-15ml为宜。少数患者在其后随访过程中行MR检查时提示残余椎体血管瘤,有行二次乙醇注射后均能很好的清除病灶。因此Hesis等学者建议注射无水乙醇法可作为治疗Ⅱ、Ⅲ型VH的一种方法。但因目前没住大样本及多中心的研究报道,并有报道VH患者术后1天内发生Brown-Squard综合征,及术后较高的病理性骨折发生率,目前单纯应用无水乙醇注射法治疗Ⅱ、Ⅲ型VH仍有争议。笔者回溯上述病例报道,发现所有病例均未从影像学上进行VH侵袭性分类,所以暂不能肯定注射乙醇后椎体病理性骨折发生率较高与治疗前椎体影响学上表现为侵袭性是否具有相关性。鉴于VH在影像学上表现为侵袭性的病灶中较易发生椎体压缩性骨折,而注射乙醇治疗法可能造成椎体骨小梁的破坏加剧,笔者建议:注射乙醇法可作为治疗IIa及IIIa型VH的一种方法;而对IIb/c及IIIb/c不建议应用。现有小样本病例报道将注射乙醇法与其他治疗方法联用。如Lonser等报道在术中病灶内注射乙醇以灭活血管瘤细胞减少术中出血,国内Chen等在椎体成型术时注射乙醇以减少复发,取得良好效果。但尚缺注射乙醇法与其他方法联合应用大样本临床研究证实其临床效果。2)动脉栓塞法(transarterial embolization):动脉栓塞法通过栓塞VH供血动脉应用于手术前以减少术中出血作为一种常规手段已经得到了较为广泛的认同。Hekster等有个例报道动脉栓塞法作为单独一种治疗非椎体压缩性骨折因素的Ⅱ、ⅢVH的手段短期内取得较好效果,动脉栓塞法治疗椎体血管瘤可能与血管堵塞,血管瘤瘤体因缺少血液充盈而收缩相关。Hekster随访一例动脉栓塞患者15年后仍无明显症状,但Smith等报道2例栓塞患者症状无明显改善。因上述病例报道缺乏长时间后续随访;VH存在与其他血管广泛联系的毛细血管网,单纯动脉栓塞法只能较大程度减少VH内血流而不能完全阻断,不能从根本上破坏VH而出现症状复发可能;同时因供血动脉栓塞可能造成相应节段的脊髓坏死等原因,单独应用动脉栓塞法目前作为治疗VH的一种常规手段在国外仍存在争议。有些学者如Reinhard等推荐动脉栓塞法单独作为一种非常规治疗方法应用于有手术禁忌及放疗禁忌的患者中,但目前暂无相关病例报道。3)经皮椎体成形法(vertebroplasty,VP):自1987年法国人Galibert等首次报道将VP应用于VH治疗中,近20年中VP治疗VH得到了快速发展。VP作为治疗目前国外Galibert等有较多文献报道应用椎体血管瘤治疗II型VH获得较好缓解疼痛的效果。VP是指经单侧或双侧椎弓根注入polymethyl methacrylate(PMMA)重塑椎体。VP治疗椎体血管瘤的缓解疼痛的机制目前尚不清楚,被认为可能与机械,化学,热量相关。PMMA可以稳定椎体,减少VH引发的远期椎体压缩性骨折;PMMA可能破坏痛觉神经末梢,提高疼痛阈值;Weill等报道未聚合的MMA对肿瘤细胞具有杀伤性。目前尚无VP治疗椎体血管瘤多中心大样本临床试验报道。但Brunot等报道VP治疗长期随访(4-10年)结果:患者疼痛症状缓解率约80-90%不等。Franc等对随访10年的VH病人连续影像学比较发现注射PMMA 10年骨水泥分布无明显变化,椎体、椎间盘及邻近椎体关节无明显影响,提示VP法作为治疗II型椎体血管瘤具有创伤较小,疼痛即刻缓解,术后复发较少等优点。椎体成形术较为严重的并发症为骨水泥泄漏,平均发生率约在1%-5%,但有报道VH病人可高达10%[68]。骨水泥泄露可能造成脊髓压迫或出血,严重时可能需要急诊手术行减压处理。肺栓塞作为VP的严重并发症已经引起重视。大部分病人发生肺栓塞时可无明显症状,因而降低了对肺栓塞发生率的估计,但Venman等报道通过肺部CT影像学检查评估VP术后病人,发现肺栓塞比例高达26%。较为少见的并发症为感染及术后一过性疼痛等。目前VP作为治疗疼痛性VH(II型)一种有效治疗手段已经得到了广泛的认同。对有脊髓压迫症状的VH,因VP可能造成压迫症状的加重,大多数学者建议将有脊髓压迫的VH(III型)作为VP治疗的相对禁忌症,但Guarnieri等有报道应用于3例有脊髓压迫症状患者,取得良好效果;Cortet等有报道VP法作为III型VH开放性手术前的一种辅助方法可在手术范围的扩大时保持椎体的相对稳定性,同时可减少术中出血。而乙醇注射法可以在消除椎体血管瘤细胞方面有较好作用,但容易诱发椎体压缩性骨折,因此国内Chen等将VP法与注射乙醇法联合应用,2年半随访后发现12例病人中仅1例症状有复发,无椎体压缩性骨折发生,但因目前应用病例数较少,尚不能确定该联合法可改善预后。4)放疗(radiotherapy):放疗作为单独或联合治疗症状性VH的一种有效方法,1929年由Baily首先应用。放疗法治疗VH机制目前尚不清楚[77]。有观点认为化疗时血管纤维化造成的循环障碍及异常血管细胞消失在其中扮演了重要角色。也有人认为大剂量的放射线造成的抗炎因子效应才是主要原因[78]。目前有较多报道放疗作为独立或者联合手段治疗VH获得较为满意的效果。2010年Heyd[77]等发布放疗治疗VH一项多中心大样本的临床治疗回溯性分析研究。资料总结了1969-2008年间作者治疗的84例病人(96个病灶,82例疼痛,24例脊髓压迫或合并疼痛),其中20例为手术后放疗,6例为栓塞后放疗,5例为椎体成型术后放疗,其余为单纯放疗,术后平均随访70月,结果单纯放疗疼痛缓解率约90%,与总体疼痛缓解率约80.9%无明显差异;同时Heyd等还回溯了1929年至2008年64例报道347个VH放疗治疗效果,疼痛缓解率约85.3%,提示放疗可作为单独或者联合治疗IIa型及IIIa型VH手段。对于放疗时的放射线剂量一直存在争议。为较好的控制症状同时尽可能减少副反应,通常认为总剂量在30-40Gy间时较为合适的。Rades等对117例放疗病人分两组进行比较研究:每次剂量约2.0Gy,总剂量应当控制在36-40Gy组病人症状控制率明显好于24-34Gy组,因此推荐总剂量36-40Gy是较为合适的放射线剂量。近期Heyd[77]等多中心研究也建议34-40Gy的总放射线剂量是较为合适的。目前单独放疗治疗非椎体压缩性原因的II型VH获得肯定,但对于III型VH应用尚存在争议。同时有学者建议将放疗作为VH次全切或椎板切除患者或者椎体成型术后的补充治疗,可以有效的缓解术后复发。放疗的副作用较少报道。较为常见的为皮肤红斑及溃疡、皮下组织纤维化、椎体骨头坏死等。罕见的并发症如神经放射性坏死,血管瘤恶变等偶有报道。Byuzadeoglu等随访VH放疗病人15年29例,未发现放疗可使病人患癌风险升高。5)手术(surgery):椎体血管瘤造成的急性、亚急性脊髓压迫(IV型)是手术减压治疗的绝对适应症。笔者回溯文献总结大部分学者在VH其余治疗无效或术后复发或者出现并发症均行手术方法治疗,并取得良好效果;对于椎体压缩性骨折引起的IIIc型VH也有较好效果。因此笔者建议IIIc型、V型可作为手术治疗的适应症。VH治疗手术方式及手术入路主要取决于VH的位置及神经压迫症状:若肿块累及全部或部分椎体,伴有或不伴有肿块突出者,可行全部或部分椎体切除重建;若VH单纯侵犯椎体后结构而无软组织肿块突出者,可单纯行全部或半侧椎板切除减压。各种手术方法各有优缺点:受累椎体肿块切除理论上可避免椎体血管瘤复发,有较多作者报道全椎板切除术术后未行化疗者随访1-4年无血管瘤复发,但因手术范围较大,尽管可术前行动脉栓塞法减少术中出血,但因手术剥离面较多,出血量仍较大,同时椎体切除可造成脊柱的不稳定性,需行椎体重建来维持椎体稳定性,手术风险及手术费用较高;单纯椎板切除减压创伤较小,手术费用相对较低,出血少,较少造成椎体不稳定,但肿块未完全切除,即使术后辅助放疗,复发概率仍较高。既往单纯手术治疗因术中出血较多;若病灶较大时为维持椎体稳定性,切除范围往往不能过大,造成术后易复发等缺点现已逐步为联合治疗所替代。联合治疗方法较多,现在多主张术前行动脉栓塞法以减少术中出血;同时也有报道术前行VP稳定椎体以减少术中出血,同时减小手术范围仅行椎板减压术取得良好效果或术中注射无水乙醇以减少术中出血等方法。肿块次全切除的病人均推荐行术后放疗治疗减少复发率。8.总结(conclusion)总体而言,目前治疗椎体血管瘤的方法较多,不同方法适用于不同类型VH,笔者总结:经皮椎体病灶内注射无水乙醇法适用于IIa、IIIa;经动脉椎体血管瘤栓塞法适用于IIa/b,IIIa/b;经皮椎体成型法适用于IIa/b/c型;放疗适用于IIa/b;手术治疗适用于IIIc、IV、V型。联合应用治疗椎体血管瘤目前已开始取得较为广泛的共识,已体现出较大的优势,可作为今后治疗椎体血管瘤的优先采用的方法。
万双林 主任医师 邵逸夫医院 骨科1.5万人已读 - 精选 骨质疏松症的药物治疗进展
摘要:骨质疏松症是一种骨量减少,骨微结构破坏,骨强度下降为特征的全身性疾病,是一种中老年人的常见病。随着社会人口老龄化的趋势,骨质疏松症的患病人数不断增加,骨质疏松症的治疗也越来越受到社会的重视。骨质
万双林 主任医师 邵逸夫医院 骨科5175人已读 - 精选 骨质疏松性腰背痛的治疗进展
一、概述骨质疏松症是一种骨量低下,骨微结构破坏,导致骨脆性增加,易发生骨折为特征的全身性骨病。2001年美国国立卫生研究院提出骨质疏松症是以骨强度下降、骨折风险性增加为特征的骨骼系统疾病,骨强度反映了骨骼的两个主要方面,即骨矿密度和骨质量。该病可发生于不同性别和任何年龄,但多见于绝经后妇女和老年男性。骨质疏松症分为原发性和继发性二大类。原发性骨质疏松症又分为绝经后骨质疏松症(Ⅰ型)、老年性骨质疏松症(Ⅱ型)和特发性骨质疏松症(包括青少年型)三种。绝经后骨质疏松症一般发生在妇女绝经后5-10年;老年性骨质疏松症一般指老人70岁以后发生的骨质疏松;而特发性骨质疏松症主要发生在青少年,病因尚不明。骨质疏松症是一个具有明确的病理生理、社会心理和经济后果的健康问题。骨质疏松症的严重后果是发生骨质疏松性骨折,这是由于骨强度下降,在受到轻微创伤或日常活动中即可发生的骨折。骨质疏松症大大增加了老年人的病残率和死亡率。疼痛、脊柱变形和发生脆性骨折是骨质疏松症最典型的临床表现。患者常表现为腰背酸痛或周身酸痛,负荷增加时疼痛加重或活动受限,严重时翻身、起坐及行走有困难。骨质疏松症引起下腰痛的可能机制:1)椎体骨小梁破坏,骨的感觉神经受到刺激;2)骨质疏松症导致骨强度下降,在受到轻微创伤情况下,便可出现椎体压缩性骨折,从而引起疼痛;3)骨质疏松患者的负重能力下降,脊柱后凸畸形,腰背肌长期处于高度紧张状态,从而出现肌肉及肌膜性腰背疼痛。临床上用于诊断骨质疏松症的通用指标是:发生了脆性骨折及/或骨密度低下,目前尚缺乏直接测定骨强度的临床手段。参照世界卫生组织推荐的诊断标准[1],基于双能X线吸收法(DXA)测定:骨密度值低于同性别、同种族健康人的骨峰值不足1个标准差属正常;降低1-2.5个标准差之间为骨量低下(骨量下降);降低等于和大于2.5个标准差为骨质疏松;骨密度降低程度符合骨质疏松诊断标准同时伴有一处或多处骨折时为严重骨质疏松。临床上常用的推荐测量部位是腰椎1-4和股骨颈,诊断时要结合临床情况进行分析。二、预防一旦发生骨质疏松性骨折,生活质量下降,出现各种并发症,可致残或致死,因此骨质疏松症的预防比治疗更为现实和重要。况且,骨质疏松症是可以预防的。骨质疏松症初级预防的对象是未发生过骨折但有骨质疏松症危险因素,或已有骨量减少者,应防止发展为骨质疏松症。预防的最终目的是避免发生第一次骨折。骨质疏松症的二级预防和治疗指已有骨质疏松症或已发生过骨折,其预防和治疗的最终目的是避免初次骨折和再次骨折。骨质疏松症的预防策略包括:1.调整生活方式1) 富含钙、低盐和适量蛋白质的均衡膳食。2) 注意适当户外活动,有助于骨健康的体育锻炼和康复治疗。3) 避免嗜烟、酗酒和慎用影响骨代谢的药物。4) 采取防止跌倒的各种措施:如注意是否有增加跌倒危险的疾病和药物,加强自身和环境的保护措施等。2.骨健康基本补充剂1) 钙剂:我国营养学会制定成人每日钙摄入推荐量800mg(元素钙),是获得理想骨峰值,维护骨骼健康的适宜剂量,如果饮食中钙供给不足可选用钙剂补充,绝经后妇女和老年人每日钙摄入推荐量为1000mg。我国老年人平均每日从饮食中获钙约400 mg,故平均每日应补充的元素钙量为500-600mg。2) 维生素D:有利于钙在胃肠道的吸收。成年人推荐剂量为200单位/d,老年人因缺乏日照以及摄入和吸收障碍常有维生素D缺乏,故推荐剂量为400-800单位/d。三、治疗1.药物治疗药物治疗适应证:已有骨质疏松症或发生过脆性骨折;或已有骨量减少并伴有骨质疏松症危险因素者。1) 抗骨吸收药物(1) 双瞵酸盐类:有效抑制破骨细胞活性、降低骨转换。目前临床上应用的阿仑磷酸钠有70mg/片(每周一次),服用方便,对消化道刺激小,有效且安全,因而有较好的依从性。密固达(唑来膦酸注射液),推荐剂量为1次静脉滴注5mg,每年1次,使用方便。(2) 降钙素类:能抑制破骨细胞的生物活性和减少破骨细胞的数量。可预防骨量丢失并增加骨量。目前临床上应用的有二种:鲑鱼降钙素和鳗鱼降钙素类似物。(3) 选择性雌激素受体调节剂:能有效抑制破骨细胞的生物活性,降低骨转换至妇女绝经前水平。目前临床上应用的有雷诺昔芬,能阻止骨丢失,增加骨密度,明显降低椎体骨折发生率,是预防和治疗绝经后骨质疏松症的有效药物,该药只用于女性患者。(4) 雌激素类:此类药物只能慎用于女性患者,抑制骨转换,阻止骨丢失。2) 促进骨形成药物:甲状旁腺激素,有促进骨形成的作用,能有效地治疗绝经后严重骨质疏松,增加骨密度,降低椎体和非椎体骨折发生的危险,因此适用于严重骨质疏松症患者。一定要在专业医师指导下应用,治疗时间不宜超过2年。3) 人工合成的锶盐雷奈酸锶,是新一代抗骨质疏松药物。同时作用于成骨细胞和破骨细胞,具有抑制骨吸收和促进骨形成的双重作用。4) 其它药物(1)活性维生素D:适当剂量的活性维生素D能促进骨形成和矿化,并抑制骨吸收。(2)维生素K2: 生成骨蛋白质,再与钙共同生成骨质,同时抑制骨基质的溶解,减少钙的流失,增加骨密度,防止骨折。(3) 中药:经临床证明有效的中成药可按病情选用。2.手术治疗随着老年人群的增加,骨质疏松性椎体骨折患者逐渐增多,因此,骨质疏松性椎体骨折日益受到人们的重视。经皮椎体成形术(Percutaneous vertebroplasty,PVP)是近年兴起的脊柱微创治疗新技术,是骨质疏松性椎体骨折治疗一大进展。 1987年由Galibert等[2]首次报告经皮穿刺椎体成形术用于椎体血管瘤的治疗,该技术能使患者迅速缓解疼痛、创伤小,尤其是治疗骨质疏松性椎体压缩骨折的一种新的、有效的微创方法。通过经皮穿刺向椎体内充填增强材料,可以达到稳定骨折、恢复椎体力学强度,防止椎体进一步塌陷和缓解疼痛的目的,使患者能够早期恢复正常活动。骨质疏松症导致椎体力学强度降低和造成椎体压缩骨折(Vertebral compression fracture,VCF), 70岁以上人群VCF发生率为20%,椎体高度降低20%或者4mm 即被认为VCF。Rao[3]将骨质疏松性椎体骨折分为3种类型:楔形压缩骨折、双凹压缩骨折和粉碎压缩骨折,其中最常见的是楔形压缩骨折(51%)。骨质疏松性椎体骨折可导致患者腰背疼痛、脊柱后凸畸形和活动减少,影响患者的呼吸、消化功能,降低生活质量。传统治疗方法如卧床休息、支具保护、口服止痛药和切开手术等,治疗效果常不甚理想。手术治疗受到内固定困难和融合效果差的限制,且骨质疏松性椎体骨折患者邻近椎体1年内再发生椎体骨折的危险性增加5-25倍[4]。疼痛缓解的可能机制:1)热学因素:骨水泥聚合时椎体中心的温度可高达112℃,使骨的感觉神经受到损伤,而椎管内温度为57 ℃; 2)化学因素:甲基丙烯酸甲酯单体具有细胞毒性,也感觉神经受到损伤;3)力学因素:内固定能使骨折部位稳定并预防其发生微动,从而限制对神经的疼痛刺激。椎体内充填增强材料有:1.甲基丙烯酸甲酯骨水泥(PMMA),其优点:1)操作方便,2)可加入不透X线材料,3)固化后强度和硬度较高,4)价格相对便宜;缺点:1)本身不具有骨传导和诱导活性,2)聚合过程温度较高,容易对周围组织造成热损伤,3)未聚合单体具有心、肺毒性,4)固化后与骨弹性模量差异较大,5)不能降解和骨替代;2.磷酸钙骨水泥(CPP)作为充填材料在恢复椎体的强度和高度方面与PMMA没有差异,其优点:1)具有骨传导活性,2)生物相容性好,3)无聚合热,4)使用安全,5)本身不透X线,是一种有潜力的椎体增强充填材料;缺点:1)流动性差,2)操作性不如PMMA,3)成骨和吸收性能尚不清楚,4)价格相对昂贵;3.硫酸钙(CS),其优点:1)具有骨传导活性,2)生物相容性好,能完全被吸收和骨替代,3)无聚合热,4)恢复椎体的强度更佳,5)不透X线材料;缺点:1)价格昂贵,2)骨替代和骨吸收迅速(10-12周)。椎体成形术可分为膨胀式椎体成形术(PVP)和球囊扩张后凸椎体成形术(Percutaneous kyphoplasty, PKP),两者均通过经皮穿刺向椎体内充填增强材料,可以达到稳定骨折、恢复椎体力学强度,防止椎体进一步塌陷和迅速缓解疼痛的目的,使患者能够早期恢复正常活动。前者在恢复椎体高度、矫正椎体后凸畸形方面的作用欠理想,但手术费用低,是后者的1/2。后者在恢复椎体高度、矫正椎体后凸畸形方面的作用理想,但手术费用昂贵、操作复杂、手术时间延长等缺点。而骨质疏松性椎体骨折患者多为老年人群,对医疗费用较敏感,往往无法支付高昂的医疗费用。因此,闭合复位辅助下的椎体成形术对骨质疏松性椎体骨折的老年人患者具有现实意义。利用过伸体位闭合复位,然后再行椎体成形术,恢复椎体力学强度,缓解疼痛,从而避免椎体进一步塌陷,使患者能够早期恢复正常活动。Lee[5]在行PVP前利用体位进行复位,可使椎体前柱高度恢复(57.1±24.8)%,中柱高度恢复(61.4±20.6)%, 后柱高度恢复(51.3±23.1)%, 后凸矫正(61.6±23.7)%,与PKP相比无显著性差异,证实闭合复位方法可以有效恢复椎体高度和矫正椎体后凸畸形。在PVP或PKP选择上,Carrino[6]认为两者都可以达到优良的治疗效果,1-2个椎体亚急性椎体压缩性骨折(3-6个月)椎体压缩40-50%时选择PKP,而对于6个月以上的慢性椎体压缩性骨折,特别椎体压缩严重的患者选择PVP。但要选择合适病例,经皮穿刺椎体成形术治疗骨质疏松性骨折的绝对禁忌症较少,只有经皮穿刺的针道存在感染是绝对禁忌症。相对禁忌症包括严重的椎体压缩骨折导致经皮穿刺困难、凝血功能异常、心肺功能不能耐受手术和麻醉、椎体后壁骨折、椎体压缩骨折导致椎管狭窄或神经受压。Alvarez[7]认为骨折椎体的MRI信号改变与治疗效果密切相关,T1加权像呈低信号,T2加权像呈高信号者,68.3%的患者取得了满意的治疗效果,只有4%的患者症状无改善。闭合复位过程中应轻柔操作,避免使患者再次出现椎体骨折和脊髓损伤。其长期的安全性和有效性尚需要进一步的临床观察。参考文献1 WHO: Guidelines for preclinical evaluation and clinical trial in osteoprorosis,1998,Geneva.2 Galibert P, Deramond H. Roast P, et al. preliminary note on the treatment of vertebral angioma by percutaneous acrylic vertebroplasty. Neurochirurgie, 1987,33:166-168.3 Rao RD, Singrakhia MD. Painful osteoporotic vertebral fracture. Pathogenesis, evaluation, and roles of vertebroplasty and kyphoplasty in its management. Bone Joint Surg (Am),2003,85:2010-2022.4 Hide IG, Gangi A. Percutaneous vertebroplasty: history, technique and current perspectives. Clin Radiol, 2004:59:461-467.5 Lee ST, Chen JF. Closed reduction vertebroplasty for the treatment of osteoporotic vertebral compression fractures. Technical note. J Neurosurg, 2004,100(4 Suppl Spine):392-396.6 Carrino JA, Chan R, Vaccaro AR. Vertebral augmentation: vertebroplasty and kyphoplasty. Semin Roentgenol,2004,39:68-84.7 Alvarez L, Perez-Higueras A, Granizo JJ, et al. Predictors of outcomes of percutaneous vertebroplasty for osteoporotic vertebral fractures. Spin,2005,30:87-92.
万双林 主任医师 邵逸夫医院 骨科6433人已读 - 精选 经皮椎体后凸成形术治疗脊柱转移瘤的现状与展望
1.概要随着老年人群的增加,疼痛性脊柱转移性肿瘤患者逐渐增多,因此,疼痛性脊柱转移性肿瘤日益受到人们的重视。疼痛性脊柱转移性肿瘤导致椎体力学强度降低和造成椎体压缩骨折(Vertebral compression fracture,VCF), 疼痛性脊柱转移性肿瘤可导致患者背部疼痛、脊柱后凸畸形和活动减少,影响患者的呼吸、消化功能及下地行走,降低生活质量。传统治疗方法如卧床休息、支具保护、口服止痛药和切开手术等,手术治疗受到内固定固定困难和融合效果差,以及患者无法耐受开放手术的打击,手术并发症多等限制。而化疗,激素治疗和放射治疗也不能恢复脊柱的稳定性。脊柱转移瘤的出现表明肿瘤为恶性,并处于晚期。多有顽固性背痛 ,脊柱稳定性丧失使患者只能卧床 ,病理性骨折可导致神经受压产生根痛和截瘫。止痛、稳定病椎、减少病理性骨折发生、避免骨折引起的神经损伤、提高生活质量是脊柱转移瘤治疗的主要目的。目前对于预期寿命大于 6个月的患者已由原来的保守治疗转向以手术为主的综合治疗[1]。1987年,法国医师Galibert等[2]报道了世界上第一例经皮椎体成形术 (percutaneous vertebroplasty , PVP),应用聚甲基丙烯酸甲 (polymethylmethacrylate ,PMMA)骨水泥经皮治疗C2椎体侵袭性血管瘤,取得良好的疗效。此后,该技术被逐渐应用于椎体骨质疏松性骨折及溶骨性椎体病变。但该技术在恢复椎体高度,纠正脊柱畸形方面效果不佳,并且骨水泥外露率较高,尤其在脊柱转移性肿瘤的治疗中,由于椎体骨壁破坏,骨水泥渗漏率可达65%,部分病例发生脑梗死及肺梗死,或者由于骨水泥渗漏压迫脊髓神经需行切开减压手术[3-5]。1998年Wong等 [6]首次实施经皮椎体后凸成形术(percutaneous kyphoplasty,PKP),经皮椎体后凸成形术是由PVP发展而来,该技术利用一可膨胀球囊将塌陷椎体复位并在椎体内创造一空间,然后将PMMA注入其内,以达到治疗效果。椎体成形术是近年来治疗骨质疏松性椎体压缩骨折和椎体肿瘤的微创方法,可以达到稳定骨折、恢复椎体力学强度,防止椎体进一步塌陷和缓解疼痛的目的,使患者能够早期恢复正常活动。经皮椎体成形术能使患者迅速缓解疼痛、创伤小,尤其是治疗骨质疏松性椎体压缩骨折的一种新的、有效的方法,同样也适用于脊柱肿瘤的治疗。该技术有恢复椎体高度、增强椎体强度、缓解患者疼痛、杀死局部肿瘤细胞等作用,在椎体转移性肿瘤的治疗中取得了良好的效果。2.适应症与禁忌症 2.1 适应症 对于椎体恶性肿瘤,只要是溶骨性的,通过椎体内注入PMMA,除可获稳定外,还可同时做肿瘤活检。其适应症为:(1)脊柱恶性肿瘤导致局部剧烈疼痛,活动受限需要卧床休息并靠止痛药缓解症状,并且无椎管内硬膜结构受侵并伴有椎体压缩性骨折时;(2)放疗或化疗后疼痛不能缓解者;(3)转移瘤所致脊柱稳定性下降者;(4)由于椎体恶性肿瘤有发生压缩性骨折的倾向,即使患者无症状 , PKP治疗仍是个较好方法。 2.2禁忌症 (1)对于对造影剂过敏患者不能用球囊扩张凸成形术(如果球囊破裂,造影剂会溢出),这类病例可以用SKy 后凸成形术治疗[7];(2)严重出凝血疾病,有造成穿刺部位血肿可能的患者应规为相对禁忌证,应用时应谨慎;(3)对于椎体后缘骨皮质完全破坏 ,骨水泥易向椎管内溢入,压迫椎管内结构者应慎用;(4)同一次手术中对3个以上椎体行PKP时,肺栓塞的风险明显增加,应视为相对禁忌症。3.填充材料PKP临床上最常用的填充物是 PMMA 骨水泥 ,但PMMA有固化时大量放热 ,发生渗漏后有灼伤邻近组织 (尤其是脊髓和神经 )的可能 ,同时也烧伤骨细胞 ,不能与骨组织生物连接、不可生物降解等诸多问题。理想的用于 PKP的充材料应具备以下特点[8]:( 1)良好的显影能力;(2) 调制简便,易于注射;(3)适宜的聚合温度;(4) 6~10min的操作时间,15min左右的凝固时间; (5)良好的生物力学特性; ( 6)无毒; (7)极好的骨传导性和骨诱导性; ( 8 )适宜的重吸收率;(9)良好的生物相容性及生物活性; (10)合理的价格;另外,填充材料应该适于作为一些药物以及生物活性因子的载体,且具有缓释的作用。目前替代PMMA的有复合骨水泥如玻璃陶瓷强化复合骨水泥 (Orthocomp)、Cortoss(Orthovia)、Hydroxy apatite composite resin(Kuraray)以及可生物降解的骨水泥如 天然珊瑚骨替代物和磷酸钙骨(Calciumphosphatecement, CPC)等[9]。复合骨水泥如Orthocomp、Cortoss、Hydroxyapathe composite resin(Kuraray)等与PMMA具有相似的基本性质,但较PMMA有更合适的粘稠度、X线的不透射性、硬化快、产热低、具有更好的力学性能、生物活性及骨诱导性等优点。磷酸钙骨水泥(CPC), 克服了PMMA的诸多缺点,具有骨传导作用、生物相容性好、易吸收、可塑形性和密封性好等优点,但其亦存在不足, 如缺乏成骨诱导活性[10 11]等。CPC 可能是椎体后凸成形术更好的注入材料, 但在体内的应用及长期生物力学和生物效应还需要进一步的研究[12]。4.操作方法手术一般采取局部麻醉,既简化手术过程,又有利于观察术中患者反应,提高安全性。在C型臂X线机监视下,通过经皮穿刺经椎弓根或椎弓根旁途径将可膨胀球囊植入塌陷的椎体,通过球囊扩张恢复椎体高度,矫正脊柱后凸畸形,并且在椎体内形成空腔,使骨水泥能在较低压力下注入椎体,填充空腔。T5-T12椎体常采用椎弓根旁途径,及经椎弓根与肋骨头间途径置入球囊,进针点位于横突和上关节突交界处,在肋横关节间稍高于椎弓根外侧壁;在T10-L5可采用经椎弓根途径,进针点位于椎弓根影外上方,左侧10点钟,右侧2点钟位置,可有效避免血管神经损伤,防止填充剂向椎旁渗漏。T 5 以上椎体椎弓根过细,无法承受 8 G 的工作套管,因而不适合PKP[13]。填充物的量:Mathis等[14]认为在胸椎内注入2~3ml ,腰椎内注入4~5ml可有效恢复椎体的抗压强度和抗张强度。Liebschner等[15]报道仅需注入椎体容量15%的灌注剂即可恢复椎体的抗压强度和抗张强度,而且经两侧椎弓根注入可使灌注剂分布更均匀,较单侧椎弓根注入能更好地恢复脊柱的稳定性。术前半小时可静脉给予抗生素,骨水泥中也可加入抗生素, Mathis常规将妥布霉素112g加入骨水泥,但没有对照实验结果证明这样可以降低感染的发病率。术后可应用抗生素软膏注入针眼,无菌绷带包扎,术后可应用2~3d抗生素[14]。5.治疗机制及临床疗效脊柱转移瘤属肿瘤晚期表现,生存期一般短暂,转移瘤的顽固性疼痛以及由此而导致的睡眠、食欲、情绪、体力等不良影响使患者生存质量严重低下,提高生存质量是脊柱转移瘤治疗的主要目的。PKP向椎体内注入的骨水泥可以渗透到骨小梁间隙硬化,使骨折部位稳定并预防其发生微动,从而减少或消除对神经的刺激,达到减轻、消除疼痛的目的[16]。另外,骨水泥的机械作用可阻断肿瘤血供,使肿瘤坏死,骨水泥聚合反应时局部温度达到 70 ℃,能直接杀灭肿瘤,并破坏感觉神经末梢[17],骨水泥单体的细胞毒性对肿瘤亦有杀灭作用,上述机制的共同作用能迅速缓解顽固性背痛,实现术后早期活动,提高生活质量。Pugmacher等[18]报告对65例脊柱转移瘤患者共99节病椎采取PKP治疗,术后疼痛缓解效果明显,2年内随访,所有存活患者疼痛无明显复发。Fourney等[19]等报道了对平均年龄为62岁的56例脊柱恶性肿瘤患者因存在长期顽固性疼痛而行椎体成形术,其中的32个病变椎体行PKP手术治疗,经术后评价、随访,84%的患者疼痛明显缓解,而且该组所有行PKP 手术患者无一例出现不良并发症。Ledlie[20]等报道了对96名患者的104节椎体行PKP 治疗的回顾分析,结果显示术后73%的患者疼痛消失,15%的患者疼痛缓解,术后椎体前部和正中线的高度分别增加了25%和27%,经过平均1年的随访,椎体高度保持稳定,行PKP治疗期间,患者平均住院时间为2天。Fourney[21]等对32例因脊柱转移性肿瘤导致压缩性骨折的椎体行PKP治疗,并随访1年,术后80%的患者疼痛完全消失,且在随访期间无复发,患者脊柱后凸角度从术前的 25.7°减小到术后的 20.5°。另外,对于脊柱转移瘤患者,大约有 20%将出现脊髓压迫[22],导致神经功能受损,出现运动及括约肌功能障碍。多个研究显示通过手术可使大多数患者的神经功能得到改善[23],术前神经功能状况是影响术后神经功能预后的最主要因素,术前神经功能受损严重的患者术后神经功能恢复状况显著不如术前神经功能受损轻微者[24]。6.并发症PKP的并发症主要为骨水泥渗漏,多数为无症状渗漏。如渗漏入椎管内或椎旁,可导致脊髓、神经根压迫症状 ;如渗漏入静脉血管,可导致肺栓塞、脑梗死等。Nussbaum等[25]回顾分析椎体后凸成形术并发症的近期相关文献和FDA报道的数据后认为,尽管此手术安全性较高,但需注意骨水泥的副反应,如低血压,在一些病例中可导致患者死亡,尤其是多椎体同时行PKP手术时;另外,可能增加椎弓根骨折的风险和改变椎间隙应力。由于球囊扩张椎体后凸成形术大部分并发症都与骨水泥渗漏到椎静脉系统有关,Groen等[26]从解剖学与生理需角度考虑,认为手术时在麻醉帮助下提高胸腔内静脉压,有利于降低此类并发症发生的风险。关于PKP是否会增加椎体再次骨折事件,目前仍存在争议。临床观察到,PKP术后患者再次出现骨折的椎体多位于先前治疗的邻近椎体,一种观点认为椎体强化后会改变脊柱生物力学性能,从而诱发邻近椎体发生骨折,骨水泥强化后的骨折椎体强度明显高于邻近未强化的椎体,两个椎体强度的较大差异可能是诱发邻近椎体骨折的重要原因之一;另一种观点认为新发的椎体骨折与强化椎体的相关性不大。患者发生了骨折,说明其本身已经处于骨折的高发状态,随后发生的骨折是其本身疾病所致,下胸椎和腰椎是骨质疏松椎体骨折的高发区,再发骨折必然集中在这个区域,与这个区域先前强化的椎体无关[27]。两种观点均需要进一步研究予以证实。7.微创治疗的联合应用1)射频消融术联合椎体成形术及局部化疗。2) 椎体成形术联合125I粒子治疗。8.总结脊柱转移瘤患者中有较多的多椎体转移病例,这需要临床医生在一次手术内处理较多的病椎,如何有效的降低多椎体PKP的骨水泥渗漏风险是需要解决的问题,现在已有的新技术如蛋壳技术、Vesse1-X骨材料填充器技术等,其效果及并发症发生率还需进一步观察。另外,PKP治疗费用较高,在我国,这也是限制PKP普及的重要因素。总体说来,PKP技术创伤小,操作较简单,能有效缓解椎体溶骨性转移瘤所致的疼痛,增加椎体强度,提高脊柱稳定性,随着填充材料及手术技术的进步,PKP将在脊柱转移瘤姑息性治疗中发挥更大的作用。9.展望脊柱转移瘤的治疗必须遵循多学科协作的原则,制定一个合适的个体化治疗方案。适合肿瘤手术切除的患者应该建议进行手术切除以提高生存率。姑息性手术目前仍是最常用的治疗手段。对于预期生存期较短的脊柱转移瘤患者,治疗的主要目标在于通过防止骨折和神经功能障碍以缓解疼痛、控制肿瘤来提高患者的生活质量。随着微创外科技术的不断发展,脊柱转移瘤患者将会有更多微创治疗方式可以选择。10.参考文献[1] Wetzel F T ,Phillip s FM. Management of metastatic disease of the spine. Ort hop Clin Nort h Am, 2000 ,31 :6112621.[2] Galibert P , Deramond H , Rosat P , et al. Preliminary note on the treatment of vertebral angioma by percutaneous acrylic vertebroplasty. Neurochirurgie , 1987 ,33 :1662168.[3] Weill A , Chias J, Simon JM ,et al. Spinal metastases indications for and results of percutoneous injection of acrylic surgical cement . Radiology ,1996 ,199 :2412247.[4] Tozzi P ,Abdelmoument Y ,Corno A F ,et al. Management of pulmonary embolism during acrylic vertebroplasty. Annals of Thoracic Surgery ,2002 ,74 :170621708.[5] Scroop R , Eskridge J , Britz GW. Paradoxical cerebral arterial embolization of cement during int raoperative vertebroplasty :case report . American Journal of Neuroradiology ,2002 ,23 :8682870.[6] Wong X,Reiley MA,Garfin S. Vertebroplasty/Kyphoplasty[J].J Women’s Imaging,2000,2:117 - 124.[7] Tong SC , Eskey CJ , Pomerantz SR , et al. " SKyp hoplas2ty" : a single institution’s initial experience[J ]. J Vasc Interv Radiol ,2006 ,17 (6) :1025[8] Lewis G1 Injectable bone cements for use in vertebrop lasty and kyphop lasty: state - of - the - art review [ J ] 1J B iomed Mater Res B App l B iomater, 2006, 76 (2) : 456 - 4681[9] Boszczyk BM, Bierschneider M, Schmid K, et al. Microsurgical interlaminary vertebroplasty and kyphoplasty for severe osteoporotic fractures. J Neurosurg, 2004, 100 ( 1 Suppl) : 32.[10] Belkoff SM,Molloy S.Temperature measurement during polyme- rization of polymethylmethacrylate cement used for vertebroplasty. Spine, 2003,28( 14) :1555.[11] Lu WW,Cheng KM,Li YW, et al. Pereutaneous vertebral fracture fixture for spinal burst fracture: an in vivo biomechanical and morphologic study. Spine, 2001, 26(24):2684.[12] Seiji T,Akihim K,Masaya Y, et al. Biomechanical evaluation of kyphoplasty and vertebroplasty with calcium phosphate cementin a simulated osteoporotic compression fracture. J Orthop Sci,2003, 8:192.[13] 许立超,肖湘生.经皮椎体后凸成形术目前存在的若干问题.介入放射学杂志, 2008,17(2):145-148.[14] Mathis J M ,Barr JD ,Belkoff SM. Percutaneous vertebroplasty : a developing standard of care for vertebral compression fractures[J ] . Am J Neuroradiol , 2001, 22 (2) :373~381[15] Liebschner MA K ,Rosenberg SW , Keaveny TM. Effects of bone cement volume and distribution on vertebral stiffness after vertebroplasty[J ] . Spine , 2001, 26 ( 6) : 1547~1554[16] Lieberman H ,Dudeney S ,Reinhardt M K et al. Initial out come and efficacy of kyphonplasty in the treatment of painful osteoporotic vertebral compression fractures. Spine ,2001, 26 (14) :1631[17] Cotton A ,Boutry N ,Cortet B et al . Percutaneous vertebroplasty : state of the art [J ] .Radiographics ,1998, 18 (2) :311~20 ; discussion 320 - 323[18] R. Pugmacher R. Taylor A. Agarwal I. et al Balloon kyphoplasty in the treatment of metastatic disease of the spine: a 2-year prospective evaluation. Eur Spine J ,2008, 17:1042–1048[19] Fourney DR ,Schomer DF ,Nader R et al .Percutaneous vertebroplasty and kyphoplasty for painful vertebral body fractures in cancer patients [J ] . J Neurosurg , 2003, 98 (1 Suppl) :21~30[20] Ledlie JT, Fenfro M. Balloon kyphoplasty: one-year outcomes invertebral body height restoration, chronic pain, and activity levels. J Neurosurg, 2003,98(1 Suppl):36-42.[21] Fourney DR, Schomer DF, Nader R, et al. Percutaneous vertebroplasty and kyphoplasty for painful vertebral body fractures in cancer patients.J Neurosurgery, 2003,98(1suppl):21-30.[22] Siegal T. Current considerations in the management of neoplastic spinal cord compression[J]. Spine,1989,14(2):223-228.[23] Patchell RA, Tibbs PA, Regine WF, et al. Direct decompressive surgical resection in the treatment of spinal cord compression caused by metastatic cancer: arandomised trial [J]. Lancet,2005, 366 (9486):643 -648.[24] 戎利民, 韩建华,等。脊柱转移性肿瘤外科治疗生存质量分析。中山大学学报(医学科学版),2008,29(6):772-776.[25] Nussbaum DA,Gailloud P,Murphy K. J Vasc Interv Radiol,2004, 15(11):1185-1192[26] Groen RJ,du Toit DF.Phillips FM,et al.Spine,2004, 29(13):1465-1471[27] Hulme PA, Krebs J, Ferguson SJ, et al. Vertebroplasty andkyphoplasty: a systematic review of 69 clinical studies [J].Spine,2006, 31:1983 - 2001.
万双林 主任医师 邵逸夫医院 骨科3435人已读 - 医学科普 什么是高位腰椎间盘突出症?怎么治疗?
高位腰椎间盘突出症(upperlumbardischerniation,ULDH)所包括的节段目前并无明确定义,一些作者认为其指L1/2和L2/3椎间盘突出,也有作者将其扩展到L3/4。另外,由于硬膜囊较大,硬膜外腔较小和血管结构等解剖学结构,高位腰椎间盘突出髓核很少突出。但是,高位腰椎由于神经结构复杂,一旦发生神经根压迫,即会出现较为严重的临床症状。 L2/3高位腰椎间盘突出一、临床特点:1.高位腰椎间盘突出症易漏诊/误诊;2.局限在大腿前方的感觉异常提示L2根受累,膝关节内侧感觉异常提示L3根受累;3.股神经牵拉试验(+)对于高位腰椎间盘突出症诊断敏感性较高。90%-97%的腰椎间盘突出症发生在下腰椎,临床医生在L4/5和L5/S1LDH的诊断方面积累了丰富经验。而高位腰椎间盘突出症(L2、L3和L4神经根受压)的临床表现、诊断要点和下腰椎明显不同,误诊/漏诊率更高。下面我们一起通过文献了解不同节段高位腰椎间盘突出症的临床表现。 二、临床表现1)L2神经根的疼痛和/或麻木区域如上图所示:L2神经根感觉支配区域主要在膝关节上方的大腿前方,不累及膝关节。2)L3神经根的疼痛和/或麻木区域如上图所示:L3神经根感觉支配区域基本都累及膝关节内侧,少数情况可累及小腿内侧。3)L4神经根的疼痛和/或麻木区域如上图所示:L4神经根感觉支配区域更加多变,大腿外侧、大腿外侧+小腿外侧、大腿外侧+小腿前方、小腿内侧+足内侧、小腿外侧+足内侧等情况均有可能。4)统计学结果-感觉异常区域如下表所示,局限在大腿前外侧区域的感觉异常提示L2神经根的敏感性100%,特异性83.7%;膝关节内侧感觉异常提示L3神经根的敏感性80%,特异性97.4%。注:GroupA指L2神经根,GroupB指L3神经根,GroupC指L4神经根。5)统计学结果-肌力、反射、试验如下表所示,股神经牵拉试验(+)对于高位LDH诊断敏感性较高(在L2和L3根>95%);在L3和L4神经根受压时,直腿抬高试验(+)亦较多;肌力下降对高位腰椎间盘突出症诊断特异性较差。总之,高位腰椎间盘突出症的感觉异常区域对于判断受累神经根有较大帮助。详细询问病史,让患者自己在腿上画出疼痛/麻木区域,是个不错的办法。不要忘记进行股神经牵拉试验。与下腰椎间盘突出症相比,因为上腰椎的神经根不支配任何特定的肌肉,仅凭症状和体征(如深腱反射)难以准确诊断,极容易造成误诊。因此,早期、全面、准确的检查诊断尤为重要!三、高位腰椎间盘突出症的解剖特点上腰椎位于胸椎和下腰椎之间,椎体横径、椎间盘厚度、横截面积自上而下逐渐增大。上腰椎管多呈卵圆形,且硬膜囊内神经组织较多,硬膜外脂肪分布少,较下腰椎管明显狭窄;下腰椎管多近似三角形和三叶形且有明显的侧隐窝,明显区别于上腰椎(如下图)。 神经根出硬膜囊后变粗,且向前、向下倾斜,但椎管横径在L2/3和L3/4节段通常只有1-2mm,由于硬膜囊间隙较小,一旦出现椎间盘突出,神经根压迫后缓冲小,囊内多条神经受压,造成较重的神经损伤,出现复杂多变的症状和体征。四、高位腰椎间盘突出症的临床诊断腰椎间盘突出是导致腰腿痛的常见原因,常见的节段是L4/5或L5/S1水平,只有1%-11%的椎间盘突出来源于L1/2、L2/3或L3/4水平。高位腰椎间盘突出症诊断对于临床医生是一个巨大的挑战,高位腰神经根病变不会出现腿部放射痛,疼痛一般放射至腹股沟或大腿前部,这种疼痛往往会随着体位的变化而不断变化。任何特定的肌力检查、皮肤感觉测试都不能准确地确诊,大多数高位腰椎间盘突出症患者棘突间侧方有局限性压痛点,存在广泛而严重的腰腿痛,但这些症状并无特异性。有学者认为股神经拉伸试验是一种很好的诊断高位腰椎间盘突出症的方法。临床上L2神经根损伤常出现膝关节近侧及大腿区域疼痛、麻木;L3神经根损伤常出现膝关节内侧区域疼痛、麻木。我们认为单独客观的神经系统检查并不能准确地识别出上腰椎神经根病变。总之,高位腰椎间盘突出症可出现不典型的腰部和腿部症状,皮肤感觉障碍以腹股沟区、股内外侧部、股前部、小腿及足内侧部多见,并有麻木、烧灼、针刺样痛感,肌力下降以髂腰肌、股四头肌、股内收肌群的肌力减退多见。患者多有股神经牵拉试验阳性,合并低位腰椎间盘突出时合并直腿抬高试验阳性。对于下腰骶神经卡压征患者,即使影像学检查下腰椎无异常,也应高度怀疑为高位腰椎间盘突出症。五、高位腰椎间盘突出症的治疗由于高、低位腰椎间盘突出常同时发生,常出现非典型的神经受压体征,保守治疗效果差。因此,一旦确诊,应首选手术治疗。出现严重临床症状,在保守治疗无效的情况下,椎间盘切除术是高位腰椎间盘突出症的首要选择。传统手术以广泛减压为前提,牺牲较多正常结构,势必造成后方组织结构破坏较多,可能导致脊柱不稳,从而增加术后腰椎不稳和腰背痛的潜在风险。近年来,脊柱内镜技术逐渐成熟,理念创新,器械不断改善,可以避免传统手术切口广泛显露、破坏骨性结构的不足,为本病的治疗开辟了新途径。许多随机对照试验已证实,与传统开放手术相比,椎间孔镜技术治疗腰椎间盘突出症有效并有更多优势。随着手术适应证的扩大,椎间孔镜技术已经引入高位腰椎间盘突出症的治疗,其安全性和有效性得到证实。六、高位腰椎间盘突出症椎间孔镜疗效及并发症传统开放手术治疗高位腰椎间盘突出症疗效大体满意,但术中须广泛的切口显露,势必破坏原有的骨性结构、椎间关节及韧带的稳定性,术后容易遗留腰背部疼痛、腰背伸无力等症状。椎间盘镜手术较传统开放手术具有切口小、组织损伤轻等优点,但仍需破坏小关节等结构易造成医源性脊柱不稳,不是治疗ULDH的最佳选择。椎间孔镜技术可在内镜下从椎间孔区进行操作,减少对脊髓的牵拉,有效降低脊髓损伤率,由于上腰椎椎间孔区域相对较大,手术操作不必行关节突成形,有效保留骨结构,尽可能保证椎体节段间的稳定性。研究报道,椎间孔镜治疗单纯高位腰椎间盘突出症临床证实是安全且有效的。 因为适应证选择、减压不充分等原因造成的孔镜术后复发,最终更改手术方案,不但耗费巨大的医疗成本,同时给患者带来身心伤害。因此,椎间孔镜治疗高位腰椎间盘突出症需准确根据适应证选择病例,同时术者要具备良好的局部解剖知识和病理状态下的神经根与椎间盘关系辨认能力,重视术中透视精确定位,精细操作,避免神经根等组织损伤,达到精准减压,并具有丰富的开放手术经验。小结高位腰椎间盘突出症的临床症状与体征是不典型的,除了完善的影像学资料,需要系统评估患者腰腿痛部位、皮肤感觉、肌力等特点,结合较为敏感的股神经牵拉试验及直腿抬高试验进一步明确责任节段。临床研究证明椎间孔镜治疗高位腰椎间盘突出症是安全且有效的,甚至在患者满意度等方面优于开放手术;但也暴露了一些缺点,如基于上腰椎相对特殊的解剖结构,存在手术视野小、减压不充分等缺点,陡峭的学习曲线需要术者具备丰富的开放手术经验和成熟的椎间孔镜技术。术前应严格把握适应证,仔细系统地评估症状和体征,术中精准减压,减少并发症,进一步提高椎间孔镜治疗高位腰椎间盘突出症的临床疗效。
 万双林 主任医师 邵逸夫医院 骨科995人已读
万双林 主任医师 邵逸夫医院 骨科995人已读 - 医学科普 腰椎间盘突出到底要不要手术?哪种手术方式好?
经典案例18岁的小王正在读高三,今年冬天却被腰腿痛折磨得苦不堪言,到医院检查后,诊断结果为“腰椎间盘突出压迫神经”。医生考虑到小王比较年轻,又要准备高考,建议先保守治疗,但小王的情况没有改善,还出现了左小腿麻木,严重影响到学习和生活。与医生商量后,小王决定动手术。大部分腰椎间盘突出患者可接受保守治疗,如药物、牵引、手法、理疗、运动等,但总有10%-20%的腰椎间盘突出症患者躲不过手术这一关。腰椎间盘突出症患者,以前大多是中老年人,但现在年轻面孔越来越多,在接受腰椎间盘手术的患者中,大约有1/10是30岁以下的年轻人。正如上述案例中提到的小王。一般来说,绝大部分腰椎间盘突出患者可以选择保守治疗,但对于以下几种情况的患者,则需要手术治疗。一、九类患者,需要手术⑴有持续的功能障碍,严重影响生活,经3-6个月非手术治疗无改善。⑵首次发作但疼痛剧烈,尤以下肢症状明显,患者难以行动和入眠,处于强迫体位者。⑶特殊类型椎间盘突出症,诸如脱垂游离型、极外侧突出型。⑷合并马尾神经严重受压,伴有相应临床表现如大小便功能障碍者。⑸出现单根神经根麻痹,出现足下垂伴有肌肉萎缩、肌力下降者。⑹合并腰椎管狭窄者。⑺合并腰椎滑脱或腰椎不稳者。⑻症状显著且反复发作,保守治疗无效者。⑼高位及巨大椎间盘突出者。二、3种手术方式,阶梯式选择目前手术治疗主要采用阶梯治疗方案,以微创化和脊柱功能重建为追求目标。所以,单纯型的腰椎间盘突出症以腿痛为主者,可以采用微创方法摘除髓核;中央型的巨大的腰椎间盘突出症并以腰腿并重者,可采用人工腰椎间盘置换术;而严重的合并有腰椎管狭窄或腰椎不稳者,可采用减压融合术。接下来就为您简单介绍几种常见的手术方法:1.微创手术椎间盘镜治疗,即经皮腰椎间盘镜髓核摘除术,是在内窥镜的监视下应用特定的手术器械来行髓核摘除或分离粘连的神经根,治疗腰椎间盘突出症的一种方法,与传统的手术方法相比具有创伤小、出血少、恢复快及最大程度地保持了脊柱的稳定等优点。但是,由于腰椎间盘镜显露的范围比较狭小,不能完全的暴露病变部位,因此在临床上某些情况时,其疗效还不如传统的手术方法。故在应用腰椎间盘镜进行治疗是要严格掌握其适应证和禁忌证。尤其适用于单侧神经根的放射痛和麻木等。微创手术主要有:显微内窥镜下椎间盘手术医生会在患者皮肤做一个约2厘米的小切口,然后置入一个直径约2厘米的管道,在管道内放入一个内窥镜。这个镜子配有灯光和微型摄像头,能将物体放大4-6倍,并清晰地显示在电视屏上。通过这些工具,医生便可以在管道内对突出的椎间盘进行切除。这种术式,又被称为显微内窥镜下椎间盘手术(MED)。经皮内镜下椎间盘切除术(PELD)内镜下显微椎间盘摘除术,是从椎间盘后方入路,需在椎板上开窗口,而有一种方法,可以直接通过脊柱侧面的椎间孔来切除突出的椎间盘组织,不需损伤椎板。这类微创手术又常指经皮内镜下椎间盘切除术(PELD),俗称椎间孔镜手术。2.开放手术由于腰椎间盘镜显露的范围比较狭小,不能完全的暴露病变部位,对于双侧有症状的中央型巨大椎间盘的处理存在困难;另外,对于老年病人,多合并有腰椎管狭窄,需要做神经根管扩大,这些都需要做传统的开放直视手术,才能够彻底解决问题。主要包括传统开放椎间盘髓核摘除术等。传统椎间盘切除术:椎间盘切除术就是通过手术方式把椎间盘切除。这是腰椎间盘突出症最经典的手术。不过别误会,椎间盘切除并不等于把整个椎间盘都给摘了,而只是切除那些突出或脱出的,并压迫脊神经的椎间盘组织,简单讲,就是摘了髓核,保留纤维环。所以,这种术式又称为髓核摘除术。这种手术创伤小,并发症少,对人体影响小,由于只切除部分椎间盘,因此有复发的可能。不过,如果严格掌握手术的适应证,复发率非常低。单纯髓核摘除术,又叫小开窗治疗,通常,在腰后方正中位置做切口,然后在病变椎间盘对应的椎板上做一个小洞(直径约1厘米),再让器械穿过这个小洞,将髓核取出来。有时,由于是双侧椎间盘突出,或有巨大的椎间盘突出等问题,医生为了能有更好的手术视野及更好地为神经减压会先切除半椎板或者全椎板。这就相当于,原来只需在椎板上开一个小窗户,现在需开一个“大椎间盘切除术:给神经减压窗户”,甚至把墙推掉,直接做个“落地窗”。腰椎间盘突出症后路经典手术在我国开展至今已逾半个世纪,根据脊椎后部结构的切除情况,分为椎板开窗术、半椎板切除术、全椎板切除术、单侧椎板并部分关节突切除术,椎间孔扩大术等手术方法。3.其他对于伴有腰椎管狭窄者同时行腰椎侧隐窝扩大术,伴有椎体不稳者行椎间融合术。对稳定和轻度不稳的病人,在摘除病变的腰椎间盘后也可以行腰椎间盘假体置换术。1)内固定融合术椎体内固定融合术,也就是常说的“打钉”。椎间盘切除后,虽然能有效缓解疼痛,但毕竟是缺了椎间盘,时间久了,椎间隙会慢慢变窄,引起神经根管狭窄,同时腰椎前部的结构应力也会进一步下降,后部结构应力上升,造成腰椎不稳。而本来是32个椎间盘兄弟齐心协力撑起脊柱,如今有人不幸“夭折”,剩下的,特别是它相邻部位的椎间盘承受的载荷就会显著增加,从而加重腰椎不稳,可以引起严重的腰痛症状。为避免术后复发,有些医生就会选择给患者做融合术。将椎间盘全部切除,然后,在两个椎体间植入骨头,来维持椎间隙的高度。由于异体骨(即别人的骨头)比较难愈合,所以选用的骨头一般取于本人的髂骨。髂骨也就是髋骨上的一部分。目前,有PEEK材料的椎间融合器,可以用术中咬除的椎板碎骨填塞后植骨,避免再凿取自体髂骨。由于骨头愈合需要较长时间,为了使患者能早期下床活动,目前,多在植骨后采用钢钉进行固定,因此内固定融合术又被俗称为“打钉”。2)腰椎间盘置换椎间盘置换即把包括髓核、纤维环在内的整个椎间盘更换成人工椎间盘。就像用人工关节替代病变的关节一样。它的优点体现在,既能重建腰椎的解剖结构,保留其运动功能,还能同时清除病变椎间盘组织,解除对神经根的力学压迫、减少自身免疫来源和退行性病变椎间盘诱发的炎症物质,从而减轻了疼痛。腰椎间盘置换术自20世纪80年代开展到现在,技术已较为成熟,复发率很低。但腰椎间盘置换术翻修困难,目前国内较少应用。三、人工腰椎间盘是什么材料?人工腰椎间盘多数是金属与非金属组合,最常用的组合采取“金属-聚合物-金属”的“三明治”设计。金属板上设计有钉、片,或有利于骨生长的多孔涂层,可使假体固定并有足够的灵活性。中间的髓核一般采用超高分子量聚乙烯,陶瓷,聚亚胺酯等材料制成。目前,也有一些仿生材料被开发出来。仿生人工椎间盘具有髓核和纤维环结构及渗透、膨胀性能,但尚未用于临床。四、术后会复发吗?首先需要了解的是“复发”这个概念,所谓的手术复发,指的是手术节段的椎间盘突出再次出现问题。试想想,腰椎间盘的髓核都摘掉了,再次突出的机会还有多少?所以,病人手术后一段时间再次出现腰腿疼,很多并不是复发,应该要区分清楚。腰腿痛再次出现可能有两个原因:一种情况是未手术的节段的椎间盘突出引起;另一种情况是同一节段同侧或另一侧出现症状,但轻微,多有受凉的病史,考虑为神经根的炎症反应,这种情况由寒冷刺激引起,热疗和口服非甾体消炎镇痛药后迅速缓解。五、术后要注意什么?手术成功后,术后的各个方面对于疾病的康复也是至关重要的。手术后应注意如下几点:1.保持平卧位2小时,不翻身,以压迫伤口,利于止血。2.术后2-3天视病人腰腿痛恢复情况,在医生和护士的指导下做功能锻炼及戴腰围离床活动。3.术后科学的饮食方法,如多食高蛋白、高热量、粗纤维、富含维生素、易消化食物,以促进切口的愈合和骨质融合,防止便秘。4.坚持腰背肌及肢体功能锻炼,早期尽量不做上身下屈及左右过度扭曲的动作,减少脊柱的活动,避免弯腰、扛物、挑担等重体力活动。避免长时间坐位、低头、突然弯腰、扭腰,持物时注意腰部、膝关节姿势,半年内不可提重物。5.出院后3个月内腰围保护,床垫最好选择软垫硬板床。6.遵医嘱定期复诊。
 万双林 主任医师 邵逸夫医院 骨科522人已读
万双林 主任医师 邵逸夫医院 骨科522人已读 - 学术前沿 最新版原发性骨质疏松症诊疗指南解读
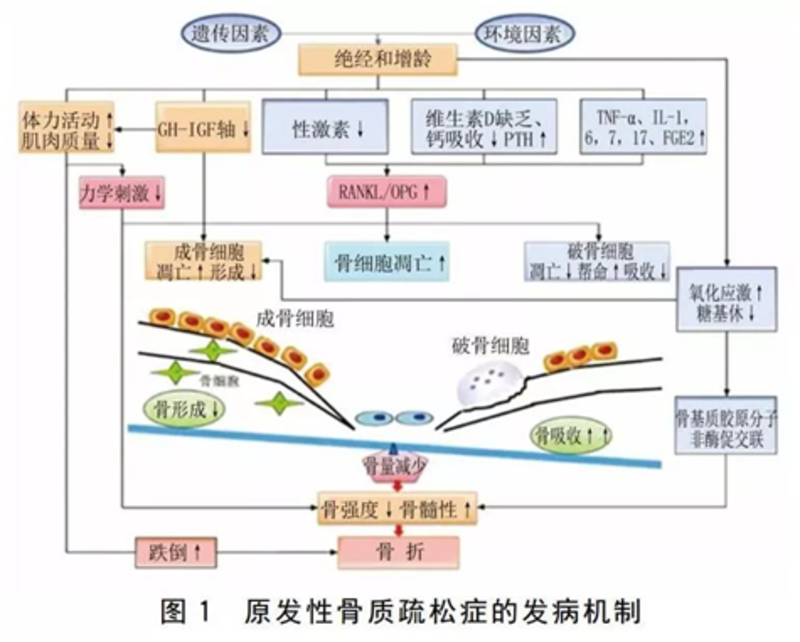
近年,由于骨质疏松症的流行病学、基础与临床研究不断探索和发现,在骨质疏松发病机制、危险因素、诊断方法与诊断标准、新药研发、分级诊疗等有了新的拓展。中华医学会骨质疏松和骨矿盐疾病分会在2011和2016年制定的原发性骨质疏松症诊疗指南基础上进行更新,现将2017年版《原发性骨质疏松症诊疗指南》(简称新指南)对旧版指南主要更新内容介绍如下。更新之一: 流行病学调查显示骨质疏松在我国中老年人口中发病率高,诊断率,治疗率低,骨折后果严重。骨质疏松症是一种与增龄相关的骨骼疾病,骨质疏松性骨折是骨质疏松症的严重后果。骨质疏松性骨折的危害巨大,是老年患者病残和致死的主要原因之一。同时,必须强调骨质疏松症是可防、可治的。需加强对危险人群的早期筛查与识别,即便已经发生过脆性骨折的患者,给予适当的治疗和康复,可有效降低再次骨折的风险。新指南建议在医疗卫生工作中重视骨质疏松症及其骨折的防治,注意识别高危人群,给予及时诊断和合理治疗。更新之二: 新增原发性骨质疏松发病机制,新指南从骨结构、骨重建机制与影响因素、力学刺激与负重、成骨细胞与破骨细胞改变、增龄、性激素变化等导致骨重建失衡、骨量丢失、骨质疏松等分子机制,阐述原发性骨质疏松(绝经后与老年性)的发病机制。新指南从骨结构、骨重建机制与影响因素、力学刺激与负重、成骨细胞与破骨细胞改变、增龄、性激素变化等导致骨重建失衡、骨量丢失、骨质疏松等分子机制,阐述原发性骨质疏松(绝经后与老年性)的发病机制,见图1。 注:RANKL:кB受体活化体配体;OPG:护骨素;TNF-α:肿瘤坏死因子α;IL:白介素;PGE2:前列腺素E2 更新之三: 骨质疏松症的危险因素,新指南将骨质疏松危险因素分为不可控因素与可控因素(旧版指南为固有因素与非固有因素),更为贴切。骨质疏松症的不可控因素与可控因素(包括不健康生活方式、疾病、药物等),见表1。 更新之四: 骨质疏松症的风险评估工具,国际骨质疏松基金会骨质疏松症风险1分钟测试题从10问增加到19问,包括不可控因素和可控因素,内容更为全面,见表2。除了危险因素的识别,还可使用工具对个体进行骨质疏松症及其骨折风险评估。新指南推荐两种骨质疏松症初筛工具:最新版国际骨质疏松基金会(IOF)骨质疏松风险一分钟测试题(表2)和亚洲人骨质疏松自我筛查工具(OSTA,表3)。后者特异性不高,且仅适合绝经后女性。 表2版国际骨质疏松基金会(IOF)骨质疏松风险一分钟测试题 表3和亚洲人骨质疏松自我筛查工具(OSTA) 注:OSTA指数=[体质量(kg)-年龄(岁)]×0.2 更新之五: 骨质疏松症的风险评估工具,新指南建议中国人群骨折风险评估测简易工具(FRAX®)预测的髋部骨折可能性≥3%或任何主要骨质疏松性骨折可能性≥20%时,为骨质疏松性骨折高危患者,建议给予治疗。此外,新指南指出跌倒是诱发骨折的重要危险因素,但FRAX®计算中没有包括跌倒。FRAX®的危险因素纳入了糖皮质激素使用史,但没有涉及糖皮质激素的治疗剂量及疗程。FRAX®也没有纳入与骨质疏松症相关的多种其他药物。FRAX®尽管列入了部分与骨质疏松症相关的疾病,包括类风湿性关节炎、糖尿病、成骨不全症等,但有待进一步完善。见表3。 更新之六: 临床表现新增骨质疏松对心理状态及生活质量的影响。指南指出:骨质疏松症及其相关骨折对患者心理状态的危害常被忽略,主要的心理异常包括恐惧、焦虑、抑郁、自信心丧失等。老年患者自主生活能力下降,以及骨折后缺少与外界接触和交流,均会给患者造成巨大的心理负担。应重视和关注骨质疏松患者的心理异常,并给予必要的治疗。令人耳目一新的是,新指南呼吁关注骨质疏松症及骨折患者的心理异常状态,并给予必要的治疗,体现了“以患者为中心”的理念。 更新之七: 骨质疏松诊断方法强调骨质疏松症诊断标准是基于双能X线吸收测定法(DXA)测量的结果。新增胸腰椎X线侧位影像和脊椎骨折评估(VFA)在骨质疏松性骨折和骨折危险人群中的应用价值。采用Genant目视半定量判定方法评估椎体压缩性骨折程度,见表4。 建议存在以下情况时,行胸腰椎侧位X线影像或VFA,以了解是否存在椎体骨折,见表5。 更新之八: 骨质疏松诊断标准,主要基于DXA骨密度测量结果和(或)脆性骨折基础上,新增基于脆性骨折的诊断判断标准,见表6。更新之九: 诊断与鉴别诊断标准愈加完善,诊断原发性骨质疏松症的思路是:确定是否为骨质疏松症,同时排除继发性骨质疏松症。在新指南中,骨质疏松症的诊断标准比以前更完善,包括三种方法,一是“金标准”双能X线吸收检测法(DXA)测定的骨密度,二是椎体和髋部脆性骨折无需依赖骨密度即可诊断,三是肱骨近端、骨盆或前臂远端发生的脆性骨折且骨密度测量符合骨量减少亦可诊断。骨形成标志物(推荐血清Ⅰ型原胶原N-端前肽,P1NP)和骨吸收标志物(推荐血清Ⅰ型胶原C-末端肽交联,S-CTX)的测定有助于鉴别原发性和继发性骨质疏松。对于前者,这些标志物水平往往正常或轻度升高,对于后者,如原发性甲状旁腺功能亢进症、某些恶性肿瘤骨转移等,标志物水平明显升高。肝肾功能、血钙磷和碱性磷酸酶、血沉、性腺激素、25羟维生素D、甲状旁腺激素、甲状腺功能等均可酌情选做,以便鉴别诊断。另外,判断骨转换类型、监测药物疗效、监测病情进展等亦能用到上述骨转换标志物。因椎体骨折无明显症状,故新指南还建议在骨质疏松性骨折的危险人群中开展椎体骨折的筛查。胸腰椎X线侧位影像可作为判定骨质疏松性椎体压缩性骨折首选的检查方法。更新之十: 骨质疏松诊断流程,新指南中,骨质疏松诊断流程新增危险因素评估和基于椎体骨折评估指证,临床诊断更为全面。更新之十一: 骨质疏松防治调整生活方式更为细化,原发性骨质疏松症分为基础治疗、药物干预和康复治疗。新指南在此方面更新完善较多,而且更规范。新指南推荐:①加强营养,均衡膳食,每日蛋白质摄入量为0.8~1.0g/kg体质量,并每天摄入牛奶300mL或相当量的奶制品;②充足日照,建议11:00~15:00,暴露四肢及面部皮肤于阳光下15~30min(取决于日照时间、纬度、季节等因素),2次/周,以促进体内维生素D的合成,尽量不涂抹防晒霜,以免影响日照效果,但需注意避免强烈阳光照射,以免灼伤皮肤;③还推荐规律的负重及肌肉力量练习,建议进行有助于骨健康的体育锻炼和康复治疗。钙剂补充方面,新指南突出选择的安全性和有效性:碳酸钙含钙量高,吸收率高,枸橼酸钙含钙量较低,但水溶性较好,胃肠道不良反应小,且枸橼酸有可能减少肾结石的发生,适用于胃酸缺乏和有肾结石风险的患者。成人推荐维生素D摄入量调整为400IU/d(旧版指南为200IU/d);65岁及以上老年人以及维生素D缺乏者,推荐摄入量调整为600IU/d(旧版指南为400-800IU/d)。 更新之十二: 骨健康基本补充剂:1.钙剂:采用2013版中国居民膳食营养素参考摄入量建议,成人每日钙推荐摄入量为800mg(元素钙),50岁及以上人群每日钙推荐摄入量为1000~1200mg,见表7。钙剂选择需考虑其钙元素含量、安全性和有效性,不同种类钙剂中的元素钙含量,见表8。 2.维生素D:采用2013版中国居民膳食营养素参考摄入量建议,成人推荐维生素D摄入量为400U(10μg)/d;65岁及以上老年人因缺乏日照以及摄入和吸收障碍常有维生素D缺乏,推荐摄入量为600U(15μg)/d;可耐受最高摄入量为2000U(50μg)/d;维生素D用于骨质疏松症防治时,剂量可为800~1200U/d。见表9。更新之十三: 骨质疏松药物干预的适应证,新指南从脆性骨则、DXA骨密度诊断骨质疏松和骨量低下3个方面阐述骨质疏松症药物干预的适应症,临床更易掌握与操作,见表10。更新之十四: 抗骨质疏松药物,新指南详尽描述目前国内抗骨质疏松药物的适应证、疗效、用法、服用方法、注意事项与禁忌证。新增骨吸收抑制剂即核因子κB受体活化因子配体(RANKL)—迪诺塞麦介绍,见表11,12。更新之十五: 用抗骨质疏松药物的临床关注问题1.关于疗程:新指南建议口服双膦酸盐治疗5年,静脉双膦酸盐治疗3年,可实施药物假期停用双膦酸盐,其间对骨折风险仍高的患者可以使用特立帕肽或雷洛昔芬;特立帕肽疗程不应超过2年;抗骨质疏松药物疗程应个体化,所有治疗应至少坚持1年,在最初3~5年治疗期后,应该全面评估患者发生骨质疏松性骨折的风险,包括骨折史、新出现的慢性疾病或用药情况、身高变化、骨密度变化、骨转换生化指标水平等;如患者治疗期间身高仍下降,则须进行胸腰椎X线摄片检查。鉴于长期使用双膦酸盐可能造成不良反应,新指南建议口服双膦酸盐治疗5年,静脉双膦酸盐治疗3年,应需考虑药物假期,对骨折风险进行评估,如为低风险,可考虑实施药物假期停用双膦酸盐;如骨折风险仍高,可以继续使用双膦酸盐或序贯其它药物。2.关于骨折后应用抗骨质疏松药物:新指南建议骨质疏松性骨折后应重视积极给予抗骨质疏松药物治疗,包括骨吸收抑制剂或骨形成促进剂等;骨质疏松性骨折后,应建议开展骨折联络服务(FLS)管理项目,促进多学科联合诊治骨质疏松性骨折,及时合理使用治疗骨质疏松症的药物,以降低再发骨折的风险3.序贯联合方案:新指南建议特别是如下情况要考虑药物序贯治疗,即某些骨吸收抑制剂治疗失效、疗程过长或存在不良反应时,以及骨形成促进剂(甲状旁腺素类似物)停药后(此类药物的推荐疗程仅为18~24个月)应序贯骨吸收抑制剂。对于抗骨质疏松症药物的使用,新指南给出明确适应证:诊断为原发性骨质疏松症者,或骨量低下且FRAX®预测的髋部骨折概率≥3%或任何主要骨质疏松性骨折概率≥20%时。对于该类药物,新指南纳入减少破骨细胞形成功能和存活的RANKL抑制剂,治疗方案更完善。新指南建议钙和维生素D联合抗骨质疏松药物治疗,不建议联合应用相同作用机制的药物。 4.中医中药治疗:新指南指出中医学文献中无骨质疏松之名,按骨质疏松症主要临床表现,中医学中相近的病证有骨痿,见于没有明显的临床表现,或仅感觉腰背酸软无力的骨质疏松患者(“腰背不举,骨枯而髓减”);骨痹,症见“腰背疼痛,全身骨痛,身重、四肢沉重难举”的患者。根据中医药“肾主骨”、“脾主肌肉”及“气血不通则痛”的理论,治疗骨质疏松症以补肾益精、健脾益气、活血祛瘀为基本治法。中药治疗骨质疏松症多以改善症状为主。新指南将国内治疗骨质疏松症的中药中药物有效成分较明确的中成药骨碎补总黄酮、淫羊藿苷和人工虎骨粉等进行了详细介绍。4.骨质疏松症防治的监测:新指南指出骨质疏松症是一种慢性疾病,其治疗是一个长期的过程,在接受治疗期间应对如下情况进行监测,即疗效、钙和维生素D的摄入是否充足、药物的不良反应、对治疗的依从性和新出现的可能改变治疗预期效果的共患病。骨质疏松症药物治疗的目的是显著提高骨强度,从而降低骨折风险。临床上,对疗效的监测受限于缺少直接检测“骨强度”的临床工具,目前可使用替代指标来监测疗效,如骨密度、骨转换标志物及脊椎影像学检查。更新之十六: 分级诊疗,新指南首次提出骨质疏松症的分级诊疗,也是一大亮点,即按照疾病的轻、重、缓、急及治疗难易程度进行分级,不同级别的医疗机构承担不同疾病状况的治疗,实现基层首诊和双向转诊,以有效利用卫生资源,做好骨质疏松症的防控和管理,同时提高医疗卫生机构开展骨质疏松症预防控制的能力,见图3。 附2017年版《原发性骨质疏松症诊疗指南》(简称新指南)概述骨质疏松症(OP)是最常见的骨骼疾病,是一种以骨量低,骨组织微结构损坏,导致骨脆性增加,易发生骨折为特征的全身性骨病。骨质疏松症可发生于任何年龄,但多见于绝经后女性和老年男性。骨质疏松症分为原发性和继发性两大类。本指南主要针对原发性骨质疏松症。 流行病学骨质疏松性骨折为受到轻微创伤或日常活动中即发生的骨折。新指南引用的最新流调数据令人忧心:2006年我国骨质疏松症患者近7000万,骨量减少者已超过2亿人,目前估测我国患者人数已远超过以上数字。2015年我国主要骨质疏松性骨折(腕部椎体和髋部)约为269万例次,2035年约为483万例次,到2050年约达599万例次,其医疗费用将分别高达720亿元、1320亿元和1630亿元。另一方面,骨质疏松症的诊断率仅为2/3左右,接受有效抗骨质疏松药物治疗者尚不足1/4。在基层医院,受检测设备、药品等因素影响,原发性骨质疏松症的诊治率极低,防治形势严峻,任重道远。 骨质疏松症危险因素骨质疏松症是一种受多重危险因素影响的复杂疾病,危险因素包括遗传因素和环境因素等多方面。骨折是骨质疏松症的严重后果,也有多种骨骼外的危险因素与骨折相关。因此,临床上需注意识别骨质疏松症及其并发症骨折的危险因素,筛查高危人群,尽早诊断和防治骨质疏松症,减少骨折的发生。骨质疏松症的危险因素分为不可控因素与可控因素,后者包括不健康生活方式、疾病、药物等(表1)。 不可控因素主要有种族、老龄化、女性绝经、脆性骨折家族史。可控因素不健康生活方式:包括体力活动少、吸烟、过量饮酒、过多饮用含咖啡因的饮料、营养失衡、蛋白质摄入过多或不足、钙或维生素D缺乏、高钠饮食、体质量过低等。影响骨代谢的疾病:包括性腺功能减退症等多种内分泌系统疾病、风湿免疫性疾病、胃肠道疾病、血液系统疾病、神经肌肉疾病、慢性肾脏及心肺疾病等。影响骨代谢的药物:包括糖皮质激素、抗癫痫药物、芳香化酶抑制剂、促性腺激素释放激素类似物、抗病毒药物、噻唑烷二酮类药物、质子泵抑制剂和过量甲状腺激素等。 骨质疏松症临床表现 1.疼痛骨质疏松症患者,可出现腰背疼痛或全身骨痛。疼痛通常在翻身时、起坐时及长时间行走后出现,夜间或负重活动时疼痛加重,并可能伴有肌肉痉挛,甚至活动受限。 2.脊柱变形严重骨质疏松症患者,因椎体压缩性骨折,可出现身高变矮或驼背等脊柱畸形。多发性胸椎压缩性骨折可导致胸廓畸形,甚至影响心肺功能;严重的腰椎压缩性骨折可能会导致腹部脏器功能异常,引起便秘、腹痛、腹胀、食欲减低等不适。 3.骨折骨质疏松性骨折属于脆性骨折,常见部位为椎体,髋部,前臂远端和肱骨近端;其他部位如肋骨、跖骨、腓骨、骨盆等部位亦可发生骨折。骨质疏松性骨折发生后,再骨折的风险显著增加。4.对心理状态及生活质量的影响骨质疏松症及其相关骨折对患者心理状态的危害常被忽略,主要的心理异常包括恐惧、焦虑、抑郁、自信心丧失等。应重视和关注骨质疏松症患者的心理异常,并给予必要的治疗。 骨质疏松症的诊断骨质疏松症的诊断基于全面的病史采集、体格检查、骨密度测定、影像学检查及必要的生化测定。临床上诊断原发性骨质疏松症应包括两方面:确定是否为骨质疏松症和排除继发性骨质疏松症。骨质疏松症的诊断主要基于DXA骨密度测量结果或脆性骨折。1)基于骨密度测定的诊断2)基于脆性骨折的诊断脆性骨折是指受到轻微创伤或日常活动中即发生的骨折。如髋部或椎体发生脆性骨折,不依赖于骨密度测定,临床上即可诊断骨质疏松症。而在肱骨近端、骨盆或前臂远端发生的脆性骨折,即使骨密度测定显示低骨量(-2.5<T-值<-1.0),也可诊断骨质疏松症。骨质疏松症的诊断标准见(表9)。骨质疏松症诊疗流程见(图4)。 骨质疏松症防治骨质疏松症的防治措施主要包括基础措施、药物干预和康复治疗。1.基础措施:包括调整生活方式和骨健康基本补充剂。调整生活方式(1)加强营养,均衡膳食:建议摄入富含钙、低盐和适量蛋白质的均衡膳食,推荐每日蛋白质摄入量为0.8~1.0g/kg体质量,并每天摄入牛奶300ml或相当量的奶制品。(2)充足日照:建议上午11:00到下午3:00间,尽可能多地暴露皮肤于阳光下晒15~30min,每周两次,以促进体内维生素D的合成,尽量不涂抹防晒霜,以免影响日照效果。但需注意避免强烈阳光照射,以防灼伤皮肤。(3)规律运动:建议进行有助于骨健康的体育锻炼和康复治疗。运动可改善机体敏捷性、力量、姿势及平衡等,减少跌倒风险。运动还有助于增加骨密度。适合于骨质疏松症患者的运动包括负重运动及抗阻运动,推荐规律的负重及肌肉力量练习,以减少跌倒和骨折风险。肌肉力量练习包括重量训练,其他抗阻运动及行走、慢跑、太极拳、瑜伽、舞蹈和兵乓球等。运动应循序渐进、持之以恒。骨质疏松症患者开始新的运动训练前应咨询临床医生,进行相关评估。(4)戒烟。(5)限酒。(6)避免过量饮用咖啡。(7)避免过量饮用碳酸饮料。(8)尽量避免或少用影响骨代谢的药物。 骨健康基本补充剂(1)钙剂:充足的钙摄入对获得理想骨峰值、减缓骨丢失、改善骨矿化和维护骨骼健康有益。(2)维生素D:充足的维生素D可增加肠钙吸收、促进骨骼矿化、保持肌力、改善平衡能力和降低跌倒风险。 2.抗骨质疏松症药物有效的抗骨质疏松症药物可以增加骨密度,改善骨质量,显著降低骨折的发生风险,本指南推荐抗骨质疏松症药物治疗的适应证(表10):主要包括经骨密度检查确诊为骨质疏松症的患者;已经发生过椎体和髋部等部位脆性骨折者;骨量减少但具有高骨折风险的患者。 双膦酸盐类 是目前临床上应用最为广泛的抗骨质疏松症药物。目前用于防治骨质疏松症的双膦酸盐主要包括阿仑膦酸钠(表12)、唑来膦酸(表13)、利塞膦酸钠(表14)、伊班膦酸钠(表15)、依替膦酸二钠(表16)和氯膦酸二钠(表17)等。 降钙素类 降钙素类药物的另一突出特点是能明显缓解骨痛,对骨质疏松症及其骨折引起的骨痛有效。目前应用于临床的降钙素类制剂有两种:鳗鱼降钙素类似物(表18)和鲑降钙素(表19)。 绝经激素治疗 绝经激素治疗(MHT)类药物(表20)能抑制骨转换,减少骨丢失,是防治绝经后骨质疏松症的有效措施。 选择性雌激素受体调节剂类 SERMs制剂雷洛昔芬(表21)在骨骼与雌激素受体结合,发挥类雌激素的作用,抑制骨吸收,增加骨密度,降低椎体骨折发生的风险。 甲状旁腺素类似物 甲状旁腺素类似物(PTHa)是当前促骨形成的代表性药物,如特立帕肽(表22),间断使用小剂量PTHa能刺激成骨细胞活性,促进骨形成,增加骨密度,改善骨质量,降低椎体和非椎体骨折的发生风险。 锶盐 雷奈酸锶(表23)是合成锶盐,体外实验和临床研究均证实雷奈酸锶可同时作用于成骨细胞和破骨细胞,具有抑制骨吸收和促进骨形成的双重作用,可降低椎体和非椎体骨折的发生风险。 活性维生素D及其类似物 活性维生素D及其类似物更适用于老年人、肾功能减退以及1α羟化酶缺乏或减少的患者,具有提高骨密度,减少跌倒,降低骨折风险的作用。 维生素K类(四烯甲萘醌) 四烯甲萘醌(表26)是维生素K2的一种同型物,是γ-羧化酶的辅酶,在γ-羧基谷氨酸的形成过程中起着重要作用。γ-羧基谷氨酸是骨钙素发挥正常生理功能所必需的,具有提高骨量的作用。 RANKL抑制剂迪诺塞麦(表27)现已被美国FDA批准治疗有较高骨折风险的绝经后骨质疏松症。 3.康复治疗针对骨质疏松症的康复治疗主要包括运动疗法、物理因子治疗、作业疗法及康复工程等。1)运动疗法运动疗法简单实用,不仅可增强肌力与肌耐力,改善平衡、协调性与步行能力,还可改善骨密度、维持骨结构,降低跌倒与脆性骨折风险等,发挥综合防治作用。运动疗法需遵循个体化、循序渐进、长期坚持的原则。治疗性运动包括有氧运动(如慢跑、游泳)、抗阻运动(如负重练习)、冲击性运动(如体操、跳绳)、振动运动(如全身振动训练)等。 2)物理因子治疗脉冲电磁场、体外冲击波、全身振动、紫外线等物理因子治疗可增加骨量;超短波、微波、经皮神经电刺激、中频脉冲等治疗可减轻疼痛;对骨质疏松骨折或者骨折延迟愈合可选择低强度脉冲超声波、体外冲击波等治疗以促进骨折愈合。神经肌肉电刺激、针灸等治疗可增强肌力、促进神经修复,改善肢体功能。联合治疗方式与治疗剂量需依据患者病情与自身耐受程度选择。3)作业疗法作业疗法以针对骨质疏松症患者的康复宣教为主,包括指导患者正确的姿势,改变不良生活习惯,提高安全性。作业疗法还可分散患者注意力,减少对疼痛的关注,缓解由骨质疏松症引起的焦虑、抑郁等不利情绪。4)康复工程行动不便者可选用拐杖、助行架等辅助器具,以提高行动能力,减少跌倒发生。此外,可进行适当的环境改造如将楼梯改为坡道,浴室增加扶手等,以增加安全性。骨质疏松性骨折患者可佩戴矫形器,以缓解疼痛,矫正姿势,预防再次骨折等。总之,骨质疏松症是慢性病,涉及骨骼、肌肉等多种组织、器官,需要综合防治。在常规药物、手术等治疗的同时,积极、规范、综合的康复治疗除可改善骨强度、降低骨折发生外,还可促进患者生活、工作能力的恢复。 综上,新指南是一部详实的临床诊疗规范,值得学习和应用。
 万双林 主任医师 邵逸夫医院 骨科2982人已读
万双林 主任医师 邵逸夫医院 骨科2982人已读 - 医学科普 怎样预防和治疗颈椎病?
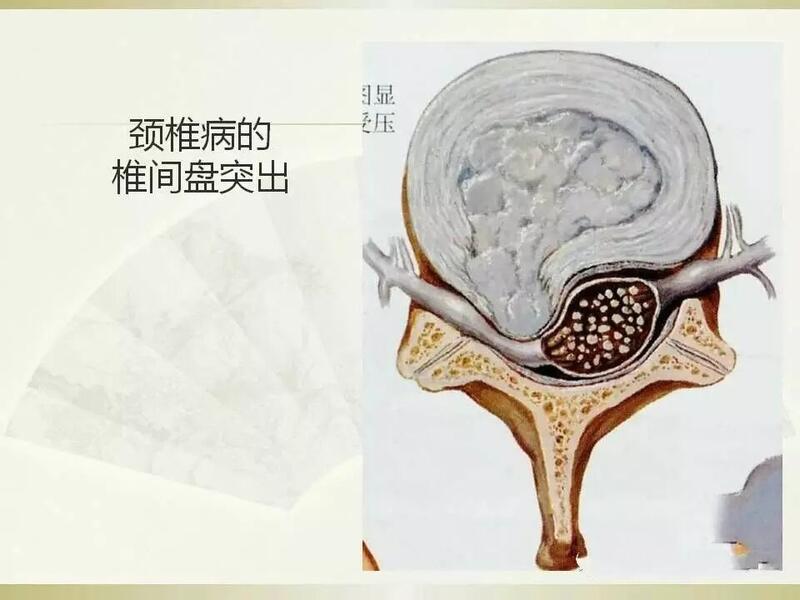
一、什么是颈椎病?颈椎病是指颈椎椎间盘退行性改变及其继发的相邻结构病理改变累及周围组织结构(神经、血管等)并出现与影像学改变相应的临床表现的疾病。二、颈椎病的发生,需满足以下3个条件:1.要有颈椎间盘的退行性改变;人类颈椎间盘在20岁左右就开始发生退变,但正常老化的椎间盘一般不会引起症状,如果在某些诱发因素下,比如慢性劳损,会明显加快椎间盘的退变,引起椎间盘的病理性改变,表现为磁共振上的“黑椎间盘”,有的会伴随颈椎间盘的突出。其中慢性劳损指超过正常生理活动范围最大限度的各种超限活动,主要有长时间低头、不良的睡姿、不恰当的颈椎活动等引起颈椎间盘的高负荷,加重椎间盘退变,也可引起颈背部肌肉的僵硬、痉挛,引起疼痛。既往颈椎病多发生于40岁以上的中老年人,但随着生活方式的改变,比如长时间低头玩手机,越来越多的年轻人患有颈椎病。2.椎间盘的退行性改变可继发其相邻结构的病理改变:比如引起骨质增生、骨刺的形成、椎间高度降低、椎管狭窄、颈椎生理弧度变直或后凸畸形等。进一步会导致椎体后方的脊髓、神经根受压,从而引起相应的症状和体征,比如颈肩部及上肢疼痛麻木、走路不稳、踩棉花感、下肢无力等。3.这些临床症状和体征必须有相应的影像学表现,且表现与临床症状相一致才能诊断为颈椎病。通俗的讲,就是患者的颈椎X线片、CT或MRI所见,可以解释患者的临床表现。有些人仅有影像学检查所见的颈椎退行性改变而无颈椎病临床症状,则不是颈椎病。同样的,具有典型颈椎病的临床表现,而影像学所见正常者,应特别注意排除其他疾患。三、为什么容易发生颈椎病?1.退行性变:退行性变指随着年龄的增长,人体各部位会出现轻重不同的老化、衰退。颈椎退行性改变是颈椎病发病的主要原因,其中椎间盘的退变尤为重要,是颈椎诸结构退变的首发因素,并由此演变出一系列颈椎病的病理解剖及病理生理改变。2.特殊的生理结构:颈椎的结构非常复杂,外有皮肤肌肉,内有韧带、骨与关节突关节;关节进一步由关节囊、滑膜、关节软骨等构成,椎间盘位于骨与骨之间,与后方的关节突关节协同起到椎间关节的作用,形成运动单位。这其中任何一个部位出现问题都有可能影响颈椎的稳定性。稳定性丧失是导致颈椎问题的关键。3.易导致颈椎受伤的行为:·1)不良的生活方式:长时间低头看书、看手机是导致颈椎病的重要原因。头部重量是很大的,在低头的时候,颈椎前屈度发生变化,使得颈椎部受到的压力过大,同时颈椎就像一个吊车,后方肌肉就是绳索,如果长期低头,后方肌肉也不免会出现劳损,久而久之,颈椎病就出现了。·2)急刹车也会导致颈椎损伤:车内的人遭遇急刹车时,由于汽车行驶的惯性,人的脖子会先前屈后弹回,犹如鞭子挥动时的反应,此时颈椎内包裹的脊髓很容易受到牵张挤压受伤,医学上称为颈椎挥鞭损伤。损伤轻者出现头晕、头痛、颈部不适等相关症状,而重者则可能导致四肢瘫痪。·尽管普遍认为脊髓的机械压迫是导致脊髓病最主要的病理生理机制,椎体间运动导致的动态压迫、先天性椎管狭窄、脊髓内形态学改变以及血管因素也参与脊髓病的进展。·静态因素:颈椎病、椎间盘退变、后纵韧带骨化、黄韧带骨化和先天性椎管狭窄。·动态因素:退行性滑脱、颈部过伸过屈时椎管的生理变窄和生理性颈部活动施加在脊髓上的应变力和拉伸力。·四、得了颈椎病,如何控制才能不加重?导致颈椎病的原因中,其中退行性变是我们无法阻止的,但是另外两点,我们在生活中完全可以进行有效控制,即增强颈椎的稳定性、杜绝不利于颈椎健康的行为。1.增强颈椎稳定性·1)缩下巴:平视前方,颈肩放松。缓慢且平稳地向后移动头部,直到不能再向后为止。当头部向后移动到最大幅度后,双手放在下巴上,辅助头部慢慢地向后推。维持3-5秒后放松。每天3-4组,每组6-8次,组间休息10秒。·2)抱头后伸:双手抱头,手指交叉,双肘张开。稍低头,用力抬头,两手向前用力,与头对抗,维持3-5秒钟后放松。每天3-4组,毎组6-8次,组间休息10秒。·3)颈部侧弯:面向前,指尖放于耳侧,头向肩部倾斜,同时用手施加阻力,维持3-5秒后慢慢回复到正中位。每天3-4组,毎组6-8次,组间休息10秒。·4)颈部前屈:面向前,指尖放于额部,头向前曲,同时用手施加阻力,维持3-5秒后慢慢抬头面向前方。每天3-4组,毎组6-8次,组间休息10秒。·5)旋转:头向前,指尖放于颞部,转头看肩,同时用手施加阻力,维持3-5秒后转回。每天3-4组,毎组6-8次,组间休息10秒。2.选择合适的枕头3.避免伤颈行为·养成良好的坐立姿势,减少长期低头的时间,如看手机可放在与视线相平行的方向。在工作中每45分钟到一个小时,活动放松5分钟。此外,注意减少颈部受凉、尽量不趴在胳膊上午睡等。·驾车时除要保持头脑清醒、时刻注意路况,且不论开车还是乘车都要紧系安全带外,最好在颈部放置头枕,预防颈椎挥鞭损伤。五、颈椎病的分型2018年发表的颈椎病专家共识,根据不同组织结构受累而出现的不同临床表现,可将颈椎病分为颈型颈椎病、神经根型颈椎病、脊髓型颈椎病和其他型颈椎病,而其中其他型涵盖既往分型中的椎动脉型和交感型颈椎病。1.颈型颈椎病颈型颈椎病实际上是各型颈椎病的早期阶段,也是最常见的一型,以青壮年居多,现在逐渐年轻化。晨起时发病多见,与枕头较高或睡姿不当有关,也常常发生于长时间低头工作或学习后。以枕、颈、肩部酸、痛、胀等不适感为主,尤其是患者常诉头颈不知放在何种位置为好,约半数患者颈部活动受限或被迫体位。查体多可见颈部肌肉僵硬,生理曲度减弱或消失,可伴颈后部明显压痛。由于颈型颈椎病的症状和体征都局限于颈部,也有学者又称为局部型颈椎病。虽然疲劳损伤或急性拉伤引起的肌肉源性颈痛是比较常见的,但是许多研究也证实椎间盘或小关节能够产生疼痛,且常引起慢性、反复、难治性慢性颈痛。主要表现为:1.患者主诉枕部、颈部、肩部疼痛等异常感觉,可伴有相应的压痛点。2.影像学检查结果显示颈椎退行性改变。3.除外其他颈部疾患或其他疾病引起的颈部症状。2.神经根型颈椎病神经根型颈椎病是较为多见的一种,常发生于C4-C7,好发节段依次是C5/6、C6/7和C4/5。多见于40~60岁人群,起病缓慢,但是也有急性发病者。以长期伏案工作、机动车驾驶员及长时间低头等不良姿势者多发。颈痛和颈部发僵,常常是最早出现的症状。有些患者还有肩部及肩胛骨内侧缘疼痛。颈椎病主要表现为从肩部沿着上臂放射至前臂或手指的疼痛、麻木(根性疼痛),夜间易犯病,有时疼痛麻木难忍,严重影响睡眠。也可有上肢肌力下降、手指动作不灵活,自觉上肢沉重感、握力减退。当头部或上肢姿势不当,或突然牵撞患肢即可发生剧烈的闪电样锐痛。颈部活动、咳嗽、喷嚏、用力及深呼吸等,可以造成症状的加重。晚期可以出现肌肉萎缩及肌束颤动。查体:颈部压痛,受累神经根所支配区域感觉改变、肌力减弱,肱二头肌、肱三头肌或桡骨膜反射活跃或减弱消失,也可有臂丛牵拉试验阳性和压颈试验阳性,但这些查体需要专业的骨科医生进行。在神经根型颈椎病中,同节段椎间盘出现问题,常引起下位神经根的受压。比如:C5神经根病常因C4-5神经根型颈椎病引起。主要表现为:1.具有较典型的神经根症状(手臂麻木、疼痛),其范围与颈脊神经所支配的区域一致,体检示压颈试验或臂丛牵拉试验阳性。2.影像学检查所见与临床表现相符合。3.除外颈椎以外病变(胸廓出口综合征、网球肘、腕管综合征、肩周炎、肱二头肌腱鞘炎及肺尖部肿瘤等)所致以上肢疼痛为主的疾患。3脊髓型颈椎病脊髓型颈椎病相对少见,但是颈椎病中最严重的一种类型。一旦延误诊治,常发展为不可逆性的神经损害。病程多慢性进展,遇诱因后加重,常有落枕史,部分人有外伤史,常与神经内科疾患混淆,甚至长期在内科治疗。临床表现多为脊髓损害的相应症状,先从下肢双侧或单侧发沉、发麻开始,随之出现行走困难,下肢肌肉发紧,抬步慢,不能快走,重者明显步态踌躇,呈宽底步态。双下肢协调差,跨越障碍物困难,双足有踩棉花样感觉。自诉颈部发硬,颈后伸时易引起四肢麻木。有时上肢症状可先于下肢症状出现,但一般略迟于下肢。上肢多一侧或双侧先后出现麻木、疼痛。严重者写字困难、饮食起居不能自理,部分有排便、排尿困难。除四肢症状外,往往有胸以下皮肤感觉减退,胸腹部发紧,临床也称之为束带感,犹如一个带子勒着胸腹部。体征最明显的是四肢张力升高,下肢多明显,多呈双侧,也可有病理征阳性,如霍夫曼征阳性。影像学多表现为脊髓明显受压的征象。主要表现为:1.临床上出现典型的颈脊髓损害的表现,以四肢运动障碍、感觉及反射异常为主。2.影像学检查所见有明确的脊髓受压征象,并与临床症状相应。3.除外肌萎缩侧索硬化症、椎管内占位、急性脊髓损伤、脊髓亚急性联合变性、脊髓空洞症、慢性多发性周围神经病等。4.其他型颈椎病该分型涵盖既往分型中的椎动脉型、交感型颈椎病。1)临床表现为眩晕、视物模糊、耳鸣、手部麻木、听力障碍、心动过速、心前区疼痛等一系列交感神经症状。体检可出现旋颈试验阳性。2)影像学表现:X线片可显示节段性不稳定;可表现为颈椎间盘退变。3)除外眼源性、心源性、脑源性及耳源性眩晕等其他系统疾病。六、颈椎病的治疗颈椎病是一种常见的颈椎间盘和椎体退行性疾病,大部分患者接受单纯保守治疗有效,但对于保守治疗无效,影响正常生活和工作的患者可行手术治疗;手术治疗方法多种多样,每一种手术方法均有其相应的适应证,手术方案的选择应考虑每个患者的临床症状、影像学表现和基础疾病,以便制订个体化的手术方案。1.保守治疗保守治疗主要适用于颈型颈椎病、神经根型颈椎病和其他型颈椎病;基本疗法包括运动疗法、物理治疗和传统医学等,具体包括颈椎牵引、颈围颈部制动、颈部理疗、改善不良体位以及可适度正规按摩等;在进行牵引、固定治疗的同时,可选择配用一些药物疗效更好,常配合应用非甾体类抗炎镇痛药、肌肉松弛剂和神经营养药等。保守治疗的基本疗法及应用原则:1)头颈牵引:以安全、有效为前提,强调小重量、长时间、缓慢、持续的原则。牵引重量为患者体重的1/12~1/14,可在牵引下进行颈背部肌肉锻炼。2)物理治疗:颈托制动、热疗、电疗等治疗方法,可能有助于改善症状。3)运动疗法:适度运动有利于颈椎康复,但不提倡使颈椎过度活动的高强度运动。4)药物疗法:非甾体类抗炎药物、神经营养药物及骨骼肌松弛类药物有助于缓解症状。5)传统医学:可予以适度按摩,但应慎重操作。手法治疗颈椎病(特别是旋转手法)有造成脊髓损伤的风险,应谨慎应用。对于疼痛反复发作、严重影响日常生活和工作的患者,可以考虑采用局部封闭或射频治疗等有创治疗方法。具备以下条件,建议采取手术治疗:(1)长期正规、系统的非手术治疗无效;(2)影像学检查有明确的病理表现(如颈椎局部不稳等);(3)责任病变部位明确。2.手术治疗1)手术适应证颈型颈椎病原则上以非手术治疗为主,对于长期非手术治疗无效而且严重影响正常生活或工作的病例可考虑手术治疗;神经根型颈椎病有明显神经根压迫症状及体征,保守治疗无效,或非手术治疗虽然有效,但反复发作而且症状严重、影响正常生活或工作;对于脊髓型颈椎病,凡是已确诊患者若无手术禁忌症,原则上应尽早手术治疗;其他型颈椎病需在多学科会诊基础上结合患者的具体情况实施。2)颈椎前路手术前路手术优点包括创伤小、手术快、出血少、恢复快,术中可直接减压、椎间融合,即刻重建颈椎稳定性,并且可恢复椎间高度,矫正矢状面平衡;前路手术分为椎间盘切除减压融合术(Anteriorcervicaldisectomyandfusion,ACDF)、椎体次全切除减压融合术(Anteriorcervicalcorpectomyandfusion,ACCF),手术在脊髓前方直接将压迫神经的椎间盘组织、骨赘或增生的纤维组织彻底切除,直接对脊髓或神经根减压;前路手术可能会出现喉返神经损伤、损伤血管气管食管、损伤颈交感干、损伤胸膜等。椎间盘切除减压融合术(ACDF)椎体次全切除减压融合术(ACCF)3)颈椎后路手术后路手术优点包括入路简单,脊髓后方间接减压,减压范围广泛,椎管成形术可保留责任节段的活动度,而且椎板切除减压术辅以钉棒系统固定可矫正颈椎曲度;后路手术分为椎板切除术(Laminectomy)、椎管成形术(Laminoplasty),其中椎管成形术可分为单开门和双开门;后路手术可能会出现轴性症状或再关门,可能与颈后韧带复合体破坏、颈椎节段性不稳、术后颈椎活动度减少、颈椎周围软组织刺激或术后长期制动等原因有关。椎管成形术4)颈椎前后路手术少数患者单纯前路手术或后路手术减压不够彻底的,需进行颈椎前后路手术。手术治疗颈椎病要遵循神经减压、重建颈椎序列稳定的手术原则,手术方式多种多样,医师需要了解不同术式的优势和劣势,严格把握不同术式的适应证和禁忌证,制订个体化的手术方案,术前周密计划,术后规范管理,减少并发症的发生。以上是一些有关颈椎病的防治知识,希望对你有所帮助,祝你早日康复!
 万双林 主任医师 邵逸夫医院 骨科128人已读
万双林 主任医师 邵逸夫医院 骨科128人已读 - 医学科普 抗骨质疏松治疗降低椎体成形术后再发椎体骨折风险
一、骨质疏松性椎体骨折椎体成形术后再发椎体骨折和新发椎体骨折我科1回顾性分析来我科就诊的椎体成形治疗疼痛性椎体骨折患者421例,356例(女283例,男73例)获得随访数据,共434个椎体数据,其中35例患者出现了术后再发椎体骨折。将35例患者分为再发骨折组,其它321例为无骨折组。将这35例再发骨折再次分组,分为邻椎骨折组和非邻椎骨折组。再发骨折组与无骨折组比较,骨密度和性别在两组中有显著性的差异。再发骨折组的平均骨密度T值为-3.95±0.59,而无骨折组中T值为-2.86±0.55(P<0.01)。再发骨折组中女性33人(94.29%),而无骨折组中女性250人(77.88%)。图为:T11,L2骨折,再发T8骨折图为:T9,T11骨折,再发T10骨折我们得出结论:女性患者和骨密度低是导致术后再发椎体骨折的主要危险因素。据报道每年大约有140万人发生骨质疏松性椎体压缩骨折(osteo-poroticvertebralcompressionfractures,OVCFs)2,经皮穿刺椎体成形术(percutaneousvertebroplasty,PVP)因其具有创伤小、迅速缓解疼痛、出血量少、安全性高、缩短住院时间、恢复正常生活快等优点,目前广泛应用于OVCFs的治疗1,3。但椎体成形术后也存在术后再发OVCFs、感染、神经根损伤、肺栓塞、骨水泥渗漏等并发症。而术后再发OVCFs严重威胁着患者的身心健康,并影响其生活质量,同时给家庭和社会带来了巨大的经济压力。二、抗骨质疏松药物对预防再发OVCFs意义重大仉培武等4通过研究证实了骨密度越低,PVP术后再发OVCFs的风险越高,因此,应用抗骨质疏松药物提高骨密度可有效预防术后再次OVCFs的发生1。一项META分析结果也提示抗骨质疏松药物的应用可降低再发OVCFs的风险5。目前可供选择的抗骨质疏松药物如下表所列,其中能快速有效提高骨密度的药物可能成为PVP术后患者的优选。RANKL抑制剂地舒单抗(Denosumab)是一种具有强效抗骨质疏松作用的人源RANKL单克隆抗体,其与人体内源性RANKL具有高亲和力,能有效抑制人体内破骨细胞的形成与激活,改善骨质疏松患者的皮质骨和松质骨强度6。上文提及META分析中5,地舒单抗可有效降低再发OVCFs风险(RR=0.41;95%CI,0.29–0.57;P<0.0001))。地舒单抗提高骨密度起效快,治疗期间疗效稳定。FREEDOM研究7中,共有7,808名(腰椎或全髋T值<-2.5且≥-4.0)的女性参与其中,地舒单抗治疗1个月,即可带来骨密度的显著提升;治疗3年,与安慰剂相比,地舒单抗治疗引起腰椎骨密度相对增加9.2%;治疗10年,与安慰剂相比,腰椎骨密度相对增加21.7%。地舒单抗还可显著降低椎体骨折风险,相比安慰剂,地舒单抗治疗第1年即可显著降低新发椎体骨折风险达61%;持续治疗3年,总体风险更可降低68%7。FREEDOM延长研究中,新发椎体骨折风险持续维持在较低水平8。地舒单抗采用皮下注射给药,任何时段都可注射,不受饮食影响,无需水化,患者无需在治疗前强制补水。有研究显示,皮下注射类药物(包含地舒单抗)相比于口服双膦酸盐类药物,降低PVP或椎体后凸成形术后再次手术率的作用更加明显(校准后sHR,0.80;95%CI,0.70-0.91;P<0.0011)9。三、总结低骨密度是骨质疏松性椎体骨折手术后再发OVCFs的重要危险因素,地舒单抗升高骨密度疗效显著,是预防PVP术后再发OVCFs,降低再次手术率的理想药物。参考文献:1.范顺武等,中华骨科杂志,2014,34(01),86-912.JohnellOetal.OsteoporosInt,2006,17(12):1726—1733.3.钟远鸣等,中国矫形外科杂志,Vol.21,No.18,Sep.2013.4.仉培武等,湖南师范大学学报(医学版),2016,13(6)5.Jin,YZ.etal.BMCMusculoskeletDisord,20(1),399.6.BoyleWJ,etal.Nature.2003;423:337-3427.CummingsSR,etal.NEnglJMed2009;361:756–658.BoneHG,etal.LancetDiabetesEndocrinol.2017Jul;5(7):513-5239.Kao,FC,etal.ClinTher,42(6),1087-1098
 万双林 主任医师 邵逸夫医院 骨科188人已读
万双林 主任医师 邵逸夫医院 骨科188人已读





